Científica Dental: abril 2021 (edición exclusiva online)
Puesta al día
Salgado Peralvo AO, Uribarri de Lucas A, Peña Cardelles JF, Castiello V, Mateos Moreno MV, Velasco Ortega E. Pautas de prescripción de antibióticos preventivos en Implantología Oral. Análisis de encuestas entre dentistas de la Unión Europea. Cient. Dent. 2021; 18; 2; 73-83
Pautas de prescripción de antibióticos preventivos en Implantología Oral. Análisis de encuestas entre dentistas de la Unión Europea
Introducción: La prescripción de antibióticos con el fin de prevenir fracasos tempranos de implantes dentales e infecciones postoperatorias supone en la actualidad un tema controvertido. El objetivo del presente estudio es el de analizar las pautas de prescripción preventiva de antibióticos en tratamientos de implantología oral entre dentistas de la Unión Europea (UE) con el fin de conocer si existe un consenso y si las recomendaciones basadas en la evidencia se están llevando a cabo.
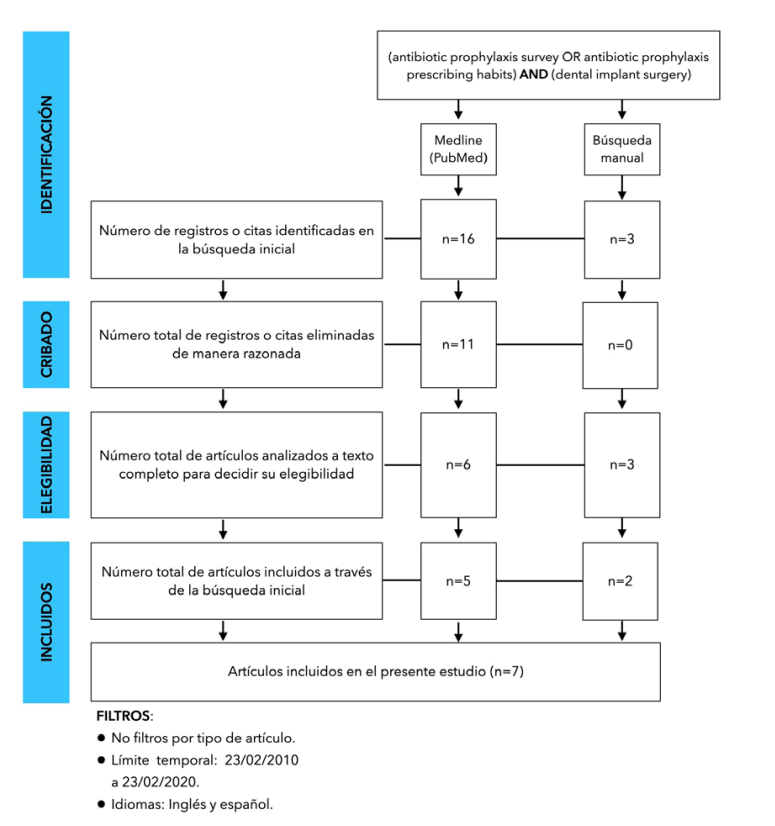
Métodos: Se realizó una búsqueda en la base de datos de MEDLINE (vía Pubmed) con los términos MeSH siguientes: “antibiotic prophylaxis survey OR antibiotic prophylaxis prescribing habits” AND “dental implant OR oral implant surgery”, de los últimos 10 años (23/02/2010 al 23/02/2020), de artículos publicados en inglés y español.
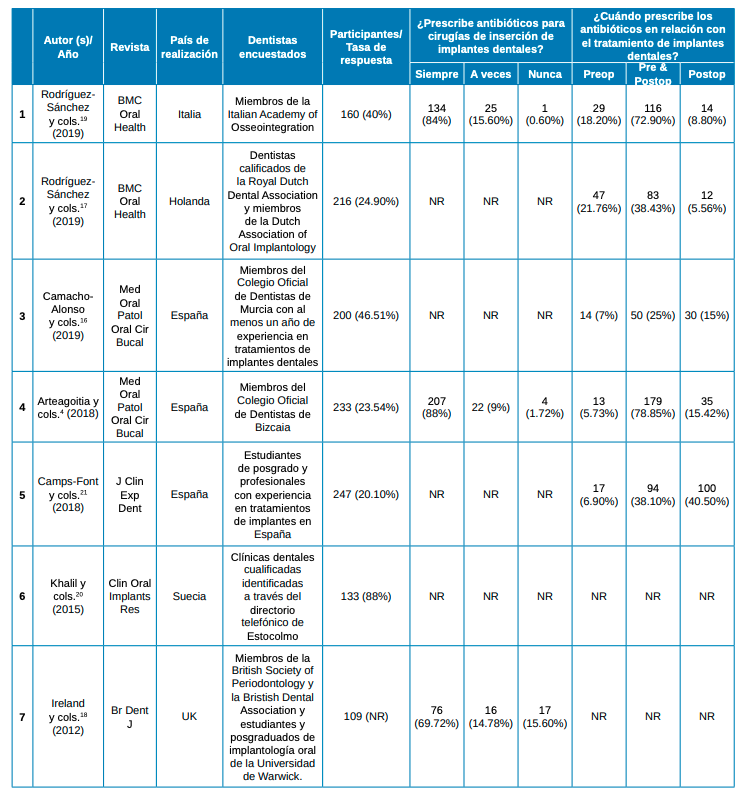
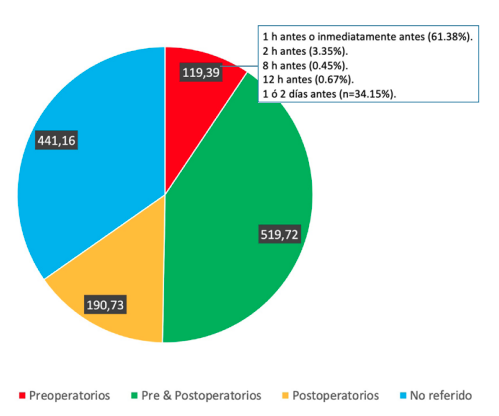
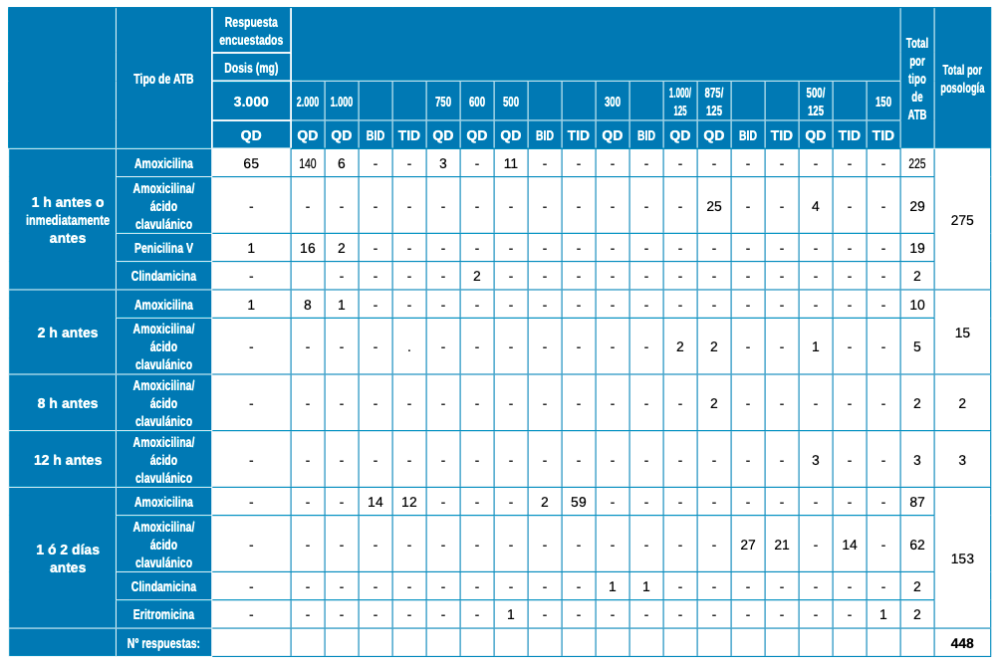
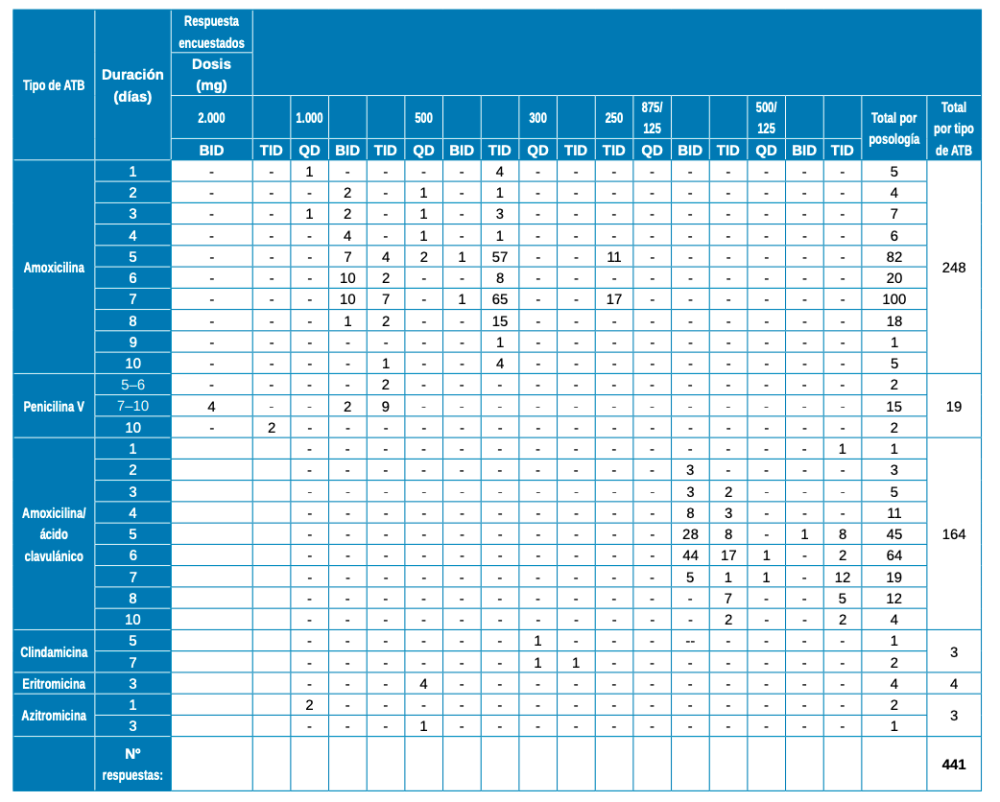
Resultados: Se incluyeron 7 estudios, dirigidos a un total de 1.271 encuestados, con unas ratios respuesta de 40.51% ± 23.23. La posología más descrita es la pre y postoperatoria (40.89%). El antibiótico más empleado en cualquiera de las pautas es la amoxicilina, seguido de amoxicilina/ ácido clavulánico.
Conclusiones: A pesar de las limitaciones de este estudio es plausible pensar que las recomendaciones basadas en la evidencia científica más actual no se están llevando a cabo. Por tanto, son necesarios protocolos que definan las indicaciones de la prescripción preventiva de antibióticos en la inserción de implantes dentales con el fin de prevenir complicaciones y/o fracasos tempranos y evitar los riesgos inherentes al uso de estos fármacos.
Introduction: Taking antibiotics to prevent early dental implant failures and postoperative infections is currently a controversial issue. The objective of this study is to analyse the guidelines for the preventive prescription of antibiotics in oral implantology treatments among dentists in the European Union (EU) to find out if there is consensus and if the evidence-based recommendations are being carried out.
Methods: A search was carried out in the MEDLINE database (via Pubmed) with the following MeSH terms: “antibiotic prophylaxis survey” OR “antibiotic prophylaxis prescribing habits” AND “dental implant OR oral implant surgery” over the last 10 years (23/02/2010 to 23/2/2020) for articles published in English or Spanish.
Results: 7 studies were included, targeting a total of 1,271 respondents, with response ratios of 40.51% ± 23.23. The dosage most described was pre- and post-operative (40.89%). The most widely used antibiotic in any of the regimens was amoxicillin, followed by amoxicillin/ clavulanic acid.
Conclusions: Despite the limitations of this study, it is reasonable to consider that recommendations based on the most current scientific evidence are not being carried out. Therefore, protocols are required to establish preventive prescription indications for antibiotics for the insertion of dental implants to prevent complications and/or early failures, as well as to minimise the risks inherent in the use of these drugs.
En los últimos años, la rehabilitación de los dientes ausentes mediante implantes dentales se ha convertido en un tratamiento común y aceptado, tanto por los pacientes como por los dentistas, principalmente debido a sus altas tasas de éxito1 . A pesar de ello, ningún procedimiento está exento de complicaciones. En este sentido, los fracasos de implantes dentales se pueden subdividir en tempranos o tardíos en función de si se producen antes o después de la carga protésica, respectivamente2 . Los fracasos tempranos constituyen un hallazgo poco común en implantología oral, con una incidencia que varía entre el 0,70 al 3,80%, dependiendo de los autores. Esta complicación se origina debido a un fracaso en la oseointegración, lo que puede estar influenciado por factores locales y/o sistémicos3 . La consecuencia final suele ser la retirada de las fijaciones. Para evitarlo se han propuesto diversos métodos preventivos como la prescripción de antibióticos4. Esto se debe a que los procedimientos óseos e implantológicos están clasificados dentro de la Clase 2 (“herida limpiacontaminada”) según la American College of Surgeons (Committee on Control of Surgical Wound Infections), caracterizados por una tasa de infección del 10-15%, sin embargo, estas cifras se pueden reducir al 1% cuando se adoptan medidas apropiadas de asepsia y se prescriben antibióticos preventivos5,6. A pesar de ello, la prescripción sistemática de antibióticos en pacientes sanos no presenta una relación riesgo-beneficio justificada7–10 y, actualmente, constituye un tema controvertido debido a la falta de consenso existente.
En 2001, surgió el proyecto llamado European Surveillance of Antimicrobial Consumption11 (ESAC), con el objetivo de controlar las resistencias bacterianas en animales y humanos. España participa activamente en este proyecto a través de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) desde que los últimos datos describieran en 2016 a España como el país con el mayor consumo de antibióticos de la Unión Europea (UE). Para prevenir las resistencias antimicrobianas, el gobierno español desarrolló el Programa de Optimización de uso de los Antibióticos (PROA)12. Dentro de sus líneas de actuación se incluye un grupo de trabajo representado por diversas sociedades científicas de dentistas que por su actividad prescriben con mayor frecuencia estos fármacos. Los dentistas desempeñan un papel clave en la prevención de este problema de Salud Pública ya que se estima que prescriben el 7–11% de los antibióticos, muchos de ellos relacionados con procedimientos de implantología oral13. En concreto, las resistencias antimicrobianas son causantes de más de 25.000 muertes al año en la UE14. Otros problemas relacionados con su consumo son la toxicidad directa, causante de problemas gastrointestinales (náuseas, vómitos, diarrea y dolor abdominal), hematológicos (neutropenia, trombocitopenia y hemolisis), alteraciones en la flora bacteriana habitual de las mucosas, que puede derivar en infecciones por cándida o colitis pseudomembranosa, nefrotoxicidad (proteinuria o fallo renal), neuropatías (disfunción nerviosa o neuropatía periférica), alteraciones hepatobiliares (ictericia o hepatitis) e interacciones medicamentosas15.
El objetivo del presente estudio es el de conocer cómo de común es la prescripción y el tipo de antibióticos preventivos empleados en tratamientos de implantología oral entre profesionales de la UE, con el fin de conocer si se está siguiendo la evidencia científica más actual.
Su M, Shi B, Zhu Y, Guo Y, Zhang Y, Xia H, et al. Comparison of implant success rates with different loading protocols: a meta-analysis. Int J Oral Maxillofac Implants 2014; 29: 344-52.
Chrcanovic B, Kisch J, Albrektsson T, Wennerberg A. Factors influencing early dental implant failures. J Dent Res 2016; 95: 995-1002.
Alsaadi G, Quirynen M, Komarek A, van Steenberghe D. Impact of local and systemic factors on the incidence of oral implant failures, up to abutment connection. J Clin Periodontol 2007; 34: 610-7.
Arteagoitia I, Rodriguez-Andres C, Rodriguez-Sanchez F. Antibiotic prophylaxis habits in dental implant surgery among dentists in Spain. A crosssectional survey. Med Oral Patol Oral Cir Bucal 2018; 23: e608-18.
Peterson LJ. Antibiotic prophylaxis against wound infections in oral and maxillofacial surgery. J Oral Maxillofac Surg 1990; 48: 617-20.
Olson M, O’Connor M, Schwartz ML. Surgical wound infections. A 5-year prospective study of 20,193 wounds at the Minneapolis VA Medical Center. Ann Surg 1984; 199: 253-9.
Ahmad N, Saad N. Effects of antibiotics on dental implants: a review. J Clin Med Res 2012; 4: 1-6.
Chrcanovic BR, Albrektsson T, Wennerberg A. Prophylactic antibiotic regimen and dental implant failure: a meta-analysis. J Oral Rehabil 2014; 41: 941-56.
Lund B, Hultin M, Tranaeus S, Naimi-Akbar A, Klinge B. Complex systematic review – Perioperative antibiotics in conjunction with dental implant placement. Clin Oral Implants Res 2015; 26: 1-14.
Salgado-Peralvo AO, Sanz-Esporrín J, Mateos-Moreno MV, Haidar-Wehbe A, Blanco-Carrión A, Velasco-Ortega E. Profilaxis antibiótica en implantología oral: Revisión crítica de la literatura. Rev Esp Cir Oral Maxilofac 2019; 41: 80-90.
Silley P, Simjee S, Schwarz S. Surveillance and monitoring of antimicrobial resistance and antibiotic consumption in humans and animals. Rev Sci Tech 2012; 31: 105- 20.
Agencia Española de Medicamentos y Productos Sanitarios. Programas de Optimización de Uso de los Antibióticos (PROA) 2017.
Goodchild JH, Donaldson M. Appropriate antibiotic prescribing for the general dentist. Gen Dent 2009; 57: 595,626,680.
ECDC/EMEA Joint Technical Report. The Bacterial Challenge: Time to React 2009.
Ziment I. Complications of antibiotic therapy. Calif Med 1972; 117: 24-48.
Camacho-Alonso F, Munoz-Camara D, Sanchez-Siles M. Attitudes of dental implantologists in Spain to prescribing antibiotics, analgesics and antiinflammatories in healthy patients. Med Oral Patol Oral Cir Bucal 2019; 24: e752-8.
Rodríguez-Sánchez F, Arteagoitia I, Rodríguez-Andrés C, Bruers J. Antibiotic prophylaxis prescribing habits in oral implant surgery in the Netherlands: a cross-sectional survey. BMC Oral Health 2019; 19: 281.
Ireland RS, Palmer NO, Lindenmeyer A, Mills N. An investigation of antibiotic prophylaxis in implant practice in the UK. Br Dent J 2012; 213: E14.
Rodriguez Sanchez F, Arteagoitia I, Rodriguez Andres C, Caiazzo A. Antibiotic prophylaxis habits in oral implant surgery among dentists in Italy: a cross-sectional survey. BMC Oral Health 2019; 19: 265.
Khalil D, Hultin M, Andersson Fred L, Parkbring Olsson N, Lund B. Antibiotic prescription patterns among Swedish dentists working with dental implant surgery: adherence to recommendations. Clin Oral Implants Res 2015; 26: 1064-9.
Camps-Font O, Viaplana-Gutierrez M, Mir-Mari J, Figueiredo R, Gay-Escoda C, Valmaseda-Castellon E. Antibiotic prescription for the prevention and treatment of postoperative complications after routine dental implant placement. A cross-sectional study performed in Spain. J Clin Exp Dent 2018; 10: e264-70.
Deeb GR, Soung GY, Best AM, Laskin DM. Antibiotic prescribing habits of oral and maxillofacial surgeons in conjunction with routine dental implant placement. J Oral Maxillofac Surg 2015; 73: 1926-31.
Abukaraky AE, Afifeh KA, Khatib AA, Khdairi NO, Habarneh HM, Ahmad WK, et al. Antibiotics prescribing practices in oral implantology among jordanian dentists. A cross sectional, observational study. BMC Res Notes 2011; 4: 266.
Romandini M, De Tullio I, Congedi F, Kalemaj Z, D’Ambrosio M, Lafori A, et al. Antibiotic prophylaxis at dental implant placement: Which is the best protocol? A systematic review and network metaanalysis. J Clin Periodontol 2019; 46: 382-95.
Singh Gill A, Morrissey H, Rahman A. A systematic review and meta-analysis evaluating antibiotic prophylaxis in dental implants and extraction procedures. Medicina (Kaunas) 2018; 54.
Esposito M, Worthington H V, Loli V, Coulthard P, Grusovin MG. Interventions for replacing missing teeth: antibiotics at dental implant placement to prevent complications. Cochrane Database Syst Rev 2010: CD004152.
Esposito M, Grusovin MG, Worthington H V. Interventions for replacing missing teeth: antibiotics at dental implant placement to prevent complications. Cochrane Database Syst Rev 2013: CD004152.
Chen Z, Chen D, Zhang S, Tang L, Li Q. Antibiotic prophylaxis for preventing dental implant failure and postoperative infection: A systematic review of randomized controlled trials. Am J Dent 2017; 30: 89-95.
Ata-Ali J, Ata-Ali F, Ata-Ali F. Do antibiotics decrease implant failure and postoperative infections? A systematic review and meta-analysis. Int J Oral Maxillofac Surg 2014; 43: 68-74.
Dajani AS, Taubert KA, Wilson W, Bolger AF, Bayer A, Ferrieri P, et al. Prevention of bacterial endocarditis: recommendations by the American Heart Association. J Am Dent Assoc 1997; 128: 1142-51.
Danda AK, Ravi P. Effectiveness of postoperative antibiotics in orthognathic surgery: a meta-analysis. J Oral Maxillofac Surg 2011; 69: 2650-6.
Kaur SP, Rao R, Nanda S. Amoxicillin: a broad spectrum antibiotic. Int J Pharm Pharm Sci 2011; 3: 30-7.
Khoury SB, Thomas L, Walters JD, Sheridan JF, Leblebicioglu B. Early wound healing following one-stage dental implant placement with and without antibiotic prophylaxis: a pilot study. J Periodontol 2008; 79: 1904-12.
Escalante MG, Eubank TD, Leblebicioglu B, Walters JD. Comparison of azithromycin and amoxicillin before dental implant placement: An exploratory study of bioavailability and resolution of postoperative inflammation. J Periodontol 2015; 86: 1190-200.
Larsson Wexell C, Ryberg H, Sjoberg Andersson WA, Blomqvist S, Colin P, Van Bocxlaer J, et al. Antimicrobial effect of a single dose of amoxicillin on the oral microbiota. Clin Implant Dent Relat Res 2016; 18: 699-706.
Maureci R, Campisi G, Matranga D, Maureci N, Pizzo G, Melilli D. The role of antibiotic prophylaxis in reducing bacterial contamination of autologous bone graft collected from implant site. Biomed Res Int 2017; 2017: 6 pages.
Aravena PC, Oyarzun CP, Arias MF, Monardes H, Jerez A, Benso B. Singledose bioavailability for prophylactic coverage in patients undergoing dental implant surgery. Int J Oral Maxillofac Implants 2018; 33: 419-24.
Patel J, Cockerill FI, Bradford P, Eliopoulos G, Hindler J, Jenkins S, et al. M07-A9: Methods for dilution antimicrobial susceptibility tests for bacteria that grow aerobically; approved Standard – tenth edition. 2015.
Vincent J, Abraham E, Kochanek P, Moore F, Fink M. Textbook of critical care. 6th edition. Philadelphia: Elsevier Health Sciences; 2011.
Blondeau JM. New concepts in antimicrobial susceptibility testing: the mutant prevention concentration and mutant selection window approach. Vet Dermatol 2009; 20: 383-96.
Classen DC, Evans RS, Pestotnik SL, Horn SD, Menlove RL, Burke JP. The timing of prophylactic administration of antibiotics and the risk of surgical-wound infection. N Engl J Med 1992; 326: 281-6.
Camps-Font O, Figueiredo R, Valmaseda-Castellon E, Gay-Escoda C. Postoperative infections after dental implant placement: Prevalence, clinical features, and treatment. Implant Dent 2015; 24: 713-9.
Hartshorne J. Do surgical prophylactic antibiotics reduce postoperative infection and early dental implant failure? Int Dent 2014; 4: 6-11.