Científica Dental: septiembre-octubre-noviembre-diciembre 2024
Revisión bibliográfica
Barrientos Moral L, Paz Cortés MM, Martín Vacas A, Aragoneses Lamas JM. Activación del eje HPA ante un agente estresante. Actualización de la determinación mediante cortisol salival. Cient. Dent. 2024; 21; 3;125-132.
Activación del eje HPA ante un agente estresante. Actualización de la determinación mediante cortisol salival
Introducción: La activación del conocido como “sistema de estrés” ante los desafíos que supone enfrentarse a la vida cotidiana actual conlleva la activación del eje HPA (hipotálamo-pituitario-adrenal) con repercusiones negativas para diversos órganos y sistemas del organismo humano, por ello se ha extendido el uso de biomarcadores sistémicos para conocer el impacto que supone el estrés en la salud general. El objetivo de esta revisión es analizar el uso del cortisol salival como respuesta sistémica a diversos agentes estresantes.
Material y métodos: Se realizó una búsqueda bibliográfica en Pubmed y Web of Science de acuerdo con criterios de inclusión y exclusión previamente establecidos.
Resultados: Fueron seleccionados un total de 28 artículos entre 2023 y 2013.
Conclusión: Tras la exposición a diferentes estresores se produce la liberación de cortisol sistémico de tal forma que éste se encuentra en la saliva en concentraciones que se asemejan a las concentraciones séricas. El uso de cortisol salival como biomarcador de estrés es un método poco invasivo válido para el estudio de la respuesta del eje HPA a estrés, pero existen diversos factores que pueden influir en la liberación de este biomarcador (edad, género, ritmos circadianos…) que deben tenerse en cuenta.
Palabras Clave: Estrés agudo; Eje HPA; Cortisol; Saliva.
Activation of the HPA axis in response to stress. Measurement by salivary cortisol
Introduction: The activation of the so-called «stress system» in the face of the challenges of coping with today’s daily life leads to activation of the HPA axis with negative repercussions for various organs and systems of the human organism, hence the widespread use of systemic biomarkers to understand the impact of stress on general health. The aim of this review is to analyse the use of salivaly cortisol as a systemic response to various stressors.
Material and methods: A literature search was carried out in Pubmed and Web of Science according to previously established inclusion and exclusion criteria.
Results: A total of 28 articles were selected between 2023 and 2013.
Conclusion: After exposure to different stressors, systemic cortisol is released in such a way that it is found in saliva in concentrations that resemble serum concentrations. The use of salivary cortisol as a stress biomarker is a low-invasive method valid for the study of the HPA axis response to stress, but there are several factors that can influence the release of this biomarker (age, sex, circadian rhythms…) that must be taken into account.
Keywords: Acute stress; HPA Axis; Cortisol; Saliva.
El término estrés fue descrito por Han Selye en 1936 como la respuesta no específica del cuerpo a cualquier demanda de cambio1. Ante la necesidad de respuesta y adaptación a un cambio, el organismo humano responde con una serie de mecanismos que activan diversos órganos y sistemas para poder hacer frente a la nueva situación, generando consecuencias positivas para la salud2. En este contexto, cabe entender que la respuesta fisiológica tras la exposición a estrés en humanos puede ser beneficiosa a corto plazo, pero hay que tener en cuenta que, mantenida en el tiempo, puede conllevar alteraciones fisiológicas en el organismo que afecten a la función de diversos órganos y sistemas, como el inmune, entre otros3. Muestra de ello es la revisión llevada a cabo por Steptoe y Kivimäki en 20124 en la que se estima que el estrés psicosocial crónico está asociado con un incremento de las enfermedades coronarias de entre un 40 y un 60%5.
El conocido como sistema de respuesta a estrés involucra tanto al eje hipotálamo-pituitario-adrenal (HPA) como al sistema nervioso simpático (SNS), y es fundamental para la supervivencia de las especies, ya que al activarse se estimulan y generan una serie de reacciones orgánicas sistémicas que logran la estabilidad del sujeto expuesto a estrés6,7. Este proceso de lograr la estabilidad a través del cambio, introducido por primera vez por Sterling y Eyer en 19888, se conoce como alostasis.
La exposición mantenida a estos desafíos o agentes estresores conlleva la liberación de una serie de mediadores fisiológicos de estrés, que puede conducir a una carga alostática caracterizada por generar un desgaste en el organismo por respuestas fisiológicas desreguladas al estrés, aumentando la posibilidad de enfermar1.
Para poder analizar la respuesta al estrés a través de biomarcadores sistémicos es importante conocer el funcionamiento del sistema de estrés. Inmediatamente después del inicio del estrés, la activación del SNS desencadena la producción de catecolaminas en la médula suprarrenal. Paralelamente, aumenta la actividad del eje HPA, de acción más lenta. Por una cascada de múltiples etapas, se observa un aumento de los corticosteroides, destacando el cortisol9 (principal hormona del eje HPA liberado por la glándula suprarrenal, se considera uno de los principales biomarcadores de estrés10). Dicha liberación se considera beneficiosa, ya que se ha asociado con la mejora del funcionamiento cardiovascular y antiinflamatorio de los sistemas inmunitarios. La desregulación de la producción de esta hormona supone un riesgo para el individuo ya que aumenta el riesgo de padecer enfermedades relacionadas con el estrés (cardiovasculares, autoinmunes,etc)7,10-12.
El cortisol desempeña una variedad de roles cruciales en la promoción de la alostasis, incluida la mediación y la supresión de respuestas saludables al estrés, pero la exposición crónica a este glucocorticoide puede provocar cambios estructurales en las regiones del cerebro responsables de modular la respuesta, como el hipocampo, y puede contribuir a la fisiopatología de la ansiedad y trastornos del estado de ánimo2,11.
Se considera que la actividad diurna de esta hormona del estrés está sujeta a la influencia de la carga alostática y al cronotipo individual. El cronotipo se relaciona con la preferencia de actividad y el ritmo circadiano conductual, así, la preferencia matutina o vespertina ha demostrado ser un rasgo estable del comportamiento humano2,14 con un impacto medible y predecible en diferentes sistemas fisiológicos y parámetros como la secreción de catecolaminas15,16.
El uso de la saliva como medio para la obtención de biomarcadores en los estudios de estrés comenzó a analizarse como alternativa poco invasiva a los métodos tradicionales en los que se utilizaban la sangre de la paciente obtenida mediante venopunción. El propio acto de la venopunción puede considerar un estrés per se y, por tanto, condicionar las mediciones de biomarcadores tras exponer al individuo al agente estresor de estudio. Múltiples estudios han validado el uso de saliva, ya que se ha observado que los niveles séricos y salivales de ciertos biomarcadores como el cortisol, están altamente correlacionados17. Esta revisión bibliográfica tiene como objetivo estudiar el uso de saliva como método de medición no invasiva de los niveles de estrés en humanos, así como los factores a tener en cuenta en cuanto a recolección de saliva, influencia de ritmos circadianos, picos de actividad del cortisol y factores que influyen en su liberación.
Se realizó una búsqueda bibliográfica en las bases de datos Pubmed y Web of Science con las palabras clave «acute stress» “hpa axis” “cortisol” y “saliva” filtrando los artículos acorde al cumplimento de los criterios de inclusión y exclusión. Se incluyeron artículos de estudios observacionales y experimentales realizados en seres humanos con medición de estrés agudo a través de cortisol salival, publicados en los últimos 10 años en revistas indexadas en JCR. Se excluyeron artículos que no cumplían los criterios de inclusión como artículos de revisión bibliográfica, en idioma diferente al español o inglés o no disponibles para lectura a texto completo, obteniendo un total de 28 artículos (Tabla 1).
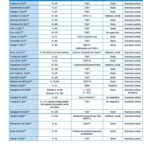
En el cuadro adjunto (Tabla 2) se observan los resultados de los artículos incluidos en esta revisión. Se incluyen únicamente los trabajos en los que los estudios cumplieran los criterios de inclusión y exclusión citados en el apartado material y método.
El tamaño muestral es muy variable entre estudios, con un rango entre 22-973 sujetos (X=135, SD ±215), en su mayoría adultos, salvo 6 estudios que incluyen menores de edad en la muestra10,18–22.
En todos los estudios incluidos en esta revisión los autores observan un cambio en las concentraciones salivales de cortisol al someter al sujeto a un agente estresante. Además, se valora la influencia de diversas variables en dicha respuesta a estrés como son el funcionamiento basal del sistema de estrés23, la habituación al agente estresor2,6,24–26, la administración de tratamientos hormonales27, factores psicosociales basales19,22,28,29, naturaleza del agente estresor30, influencia del estrés en otras tareas cognitivas31, el género25,32 la influencia del estrés acumulado7,33, cronotipo15, así como la lengua materna34.
Todos los trabajos incluidos optan por un agente estresor de naturaleza cognitiva, la mayoría de ellos, utilizan protocolos validados como agentes estresores (TSST, SECTP, MAST) siendo el Trier Social Stress Test (TSST) el más utilizado2,6,7,10,15,19,22–28,30,32–36. El TSST es un protocolo de inducción de estrés que consiste en un periodo de anticipación de 10 minutos y un periodo de test de 10 minutos en el que los sujetos tienen que llevar a cabo un discurso y realizar cálculos mentales en frente de una audiencia37. El Socially Evaluated Colp Pressor Test (SECTP)38 consiste en introducir la mano en agua helada (2ºC) tanto tiempo como sea posible hasta un máximo de 3 minutos mientras el sujeto es grabado y monitorizado de cerca por un investigador que muestra falta de empatía. El Maastricht Acute Streess Test (MAST)39 incluye la parte física del SECTP y la evaluación social y el componente mental aritmético del TSST.
Solo tres estudios incluyen un grupo control (sin estrés) frente al grupo sometido al agente estresor20,35,40.
La mayoría de los estudios realizan tanto el protocolo de estrés como la recogida de muestra por la tarde2,6,10,15,18,23–25,27,30,31,33,35,36 mientras que sólo tres lo hacen por la mañana20,21,41, a tener en cuenta a la hora de interpretar los datos debido a los ritmos circadianos que afectan a la liberación de cortisol.
Todos ellos miden la concentración de cortisol salival en distintos momentos pre y post agente estresor, además, algunos también evalúan el tiempo de recuperación del cortisol a niveles basales18,35.
En todos los estudios incluidos en esta revisión existe un aumento en los niveles de cortisol tras exponer al sujeto a un agente estresor agudo, coincidiendo la mayoría en que el pico máximo de concentración de cortisol salival se da entre los 20 y los 30 minutos posteriores a la exposición al agente causante. Sin embargo, autores como Lam y cols.33, Obasi y cols.10 e Hidalgo y cols.35 consideran que el mayor pico de cortisol se produce 10-15 minutos después de la exposición al estresor.
Para evitar la influencia de los ritmos circadianos del cortisol, la mayoría de los estudios incluidos toman las muestras salivales desde el mediodía hasta la tarde, evitando la liberación aumentada de cortisol tras despertar, excepto Mezzulo y cols.21 que lo llevaron a cabo entre las 8.30 a.m. y las 12 p.m., y Roos y cols.20 que obtuvieron sus muestras entre las 9 a.m. y 3 p.m. En el estudio de Hostinar y cols.18 comenzaron la recogida por la mañana a las 11.00 a.m. pero finalizaban por la tarde, a las 5.00 p.m.
Aunque la literatura respalda el uso del cortisol salival como biomarcador para medir la influencia del estrés en el organismo, hay diferencias interindividuales que se deben considerar para optimizar el uso de este glucocorticoide salival como biomarcador de estrés. En primer lugar, la edad, a pesar de que los primeros estudios de estrés proponían que el envejecimiento pudiese venir acompañado de cambios en la resiliencia del eje HPA, estudios recientes muestran controversia, ya que autores como Obasi y cols.10 y Lam y cols.33 muestran que la edad no se relaciona con los niveles de cortisol. Otros autores como Hidalgo y cols.35 al comparar grupos de edad encontraron que el grupo de mayor edad tenía niveles de cortisol más bajos frente al grupo más joven. McInnis y cols.24 encontraron una asociación negativa entre la edad y los aumentos de cortisol tras exposición repetida a estrés, similar con lo obtenido por Plieger y cols.31.
Por otro lado, se ha evaluado en la bibliografía la relación de los biomarcadores asociados al género. Autores como Richardson y cols.40, Herbison y cols.27 e Hidalgo y cols.35 coinciden en que los hombres mostraban una mayor activación del cortisol que las mujeres. Sin embargo, otros como Sandner y cols.9 y Thoma y cols.25 no encontraron diferencias de género en las respuestas de cortisol, al igual que Lam y cols.33. Cabe destacar que el estudio de Obasi y cols.10 encontró que los hombres tenían niveles más bajos de cortisol basal.
Con respecto a la adaptación del eje HPA al agente estresante, autores como Chen y cols.2 observaron que, tras exponer por segunda vez al sujeto al mismo estresor, la respuesta del cortisol fue significativamente menor que la respuesta inicial, al igual que Thoma y cols.25 o Manigault y cols..26. Gianferante y cols.6 encontraron menor habituación en jóvenes, por lo sugieren que la habituación pueda verse afectada por la edad y por el género, como encontraron McInnis y cols.24 con una mayor habituación en hombres que en mujeres.
Otro factor para tener en cuenta es la tendencia conductual de cada individuo. En lo referido a estrés, se ha definido como la tendencia de un individuo a reflexionar sobre una experiencia estresante, en lugar de involucrarse en otro estilo de afrontamiento, como distraerse del factor estresante. Gianferante y cols.6 vieron en su estudio que este pensamiento se asoció con una capacidad reducida para adaptarse al estrés repetido, disminuyendo la habituación del eje HPA. Finke y cols.29 desarrollaron un estudio en el que los sujetos fueron valorados positiva o negativamente (feedback positivo o negativo) tras somerterlos a un agente estresante y encontraron que los participantes sometidos a feedback negativo mostraron cortisol inicial significativamente más alto.
Autores como Fiksdal y cols.28 sugieren que tanto los síntomas depresivos como los de ansiedad pueden ser suficientes para comenzar alteraciones potencialmente dañinas en el funcionamiento del eje HPA en respuesta al estrés agudo, ya que en sus resultados obtuvieron que los síntomas depresivos parecían estar asociados a respuestas más elevadas de cortisol. Respecto a los factores emocionales, cabe señalar el estudio llevado a cabo por Guo y cols.19 en el que valoraron la influencia del apoyo emocional de padres a hijos en la respuesta a estrés, encontrando que las respuestas de los padres que no brindaban apoyo se asociaron con una menor reactividad al cortisol y mayores emociones negativas ante una tarea de estrés psicosocial.
Young y cols.7 estudiaron en niños y adolescentes la influencia de la exposición temprana a estrés o incorporación acumulativa a estrés y encontraron que la aparición de estrés en edades tempranas, así como el estrés acumulado condujeron a respuestas de cortisol atenuadas.
Los estados hormonales endocrinos manifestados como exceso de hormonas sexuales que suceden comúnmente en la adolescencia, pueden condicionar la respuesta a estrés mediante liberación de cortisol. Así, Mezzulo y cols.21 encontraron que se produjo un aumento significativo en los niveles de cortisol y cortisona salival en adolescentes que presentaban excesos de andrógenos. Del mismo modo, cabe destacar que Herbison y cols.27 encontraron niveles elevados de cortisol plasmático en mujeres que tomaban anticonceptivos orales en comparación con mujeres que no los tomaban.
El cronotipo, entendido como tendencia matutina o vespertina del cortisol, influye en la respuesta a estrés tal y como indican de Punder y cols.15 que encontraron que la tendencia vespertina se asoció con una respuesta de cortisol inducida por estrés más alta. Además, observaron que los individuos con tendencia nocturna tenían un índice de masa corporal (IMC) más alto. A pesar de que se ha estudiado la influencia del IMC en respuesta a estrés, los estudios incluidos en esta revisión no encuentran diferencias reseñables en la respuesta a cortisol respecto a este factor, salvo de Punder y cols.15, cuyos resultados sugieren que la relación entre el cronotipo y el IMC está mediada por una concentración elevada de proteína C-reactiva y que esta relación mediada es más fuerte en individuos con una respuesta de cortisol aumentada.
Otro factor que destacan diversos autores es el llamado estrés percibido, es decir, la experiencia subjetiva de estrés, ya que no todos los individuos perciben y experimentan con la misma intensidad la experiencia estresante. Obasi y cols.10 encontraron que el estrés percibido tuvo una relación inversamente significativa con los niveles basales de cortisol.
Por último, hay que destacar que la actividad basal del eje HPA muestra diferencias interindividuales e intraindividuales en función de todos los factores expuestos y por ello, individuos que muestren mayores respuestas basales del eje HPA, experimentarán respuestas más acentuadas con mayor liberación de cortisol al exponerles a agentes estresantes agudos2.
A pesar de que diversos estudios han establecido que la relación entre las concentraciones séricas y salivales de cortisol son similares41,43,44, la concentración máxima de cortisol en la saliva puede ser más tardía que en suero, obteniendo el pico en saliva aproximadamente 30 minutos más tarde respecto al suero41,43. La correlación entre las concentraciones de cortisol en saliva y suero se producen especialmente a corto plazo, como es el caso de la activación del eje HPA tras un estresor agudo, sin embargo, a largo plazo se observan discrepancias entre ambas44.
La presente revisión bibliográfica muestra evidencias que justifican el uso de saliva como medio de análisis de biomarcadores salivales de estrés, particularmente el cortisol, ya que a pesar de que existe cierta discrepancia, la literatura apoya que el pico máximo de cortisol se produce entre los 15 y los 30 minutos posteriores a la exposición al estresor. Es necesario tener en cuenta que existen diversas variables que afectan a la liberación de cortisol y, por tanto, a su utilización como biomarcador de actividad del eje HPA.
Baik JH. Stress and the dopaminergic reward system. Stress and the dopaminergic reward system. Exp Mol Med. 2020;52(12):1879-1890.
Chen X, Gianferante D, Hanlin L, et al. HPA-axis and inflammatory reactivity to acute stress is related with basal HPA-axis activity. Psychoneuroendocrinology. 2017 78:168-176.
Goetz SMM, Lucas T. C-reactive protein in saliva and dried blood spot as markers of stress reactivity in healthy African-Americans. Biomark Med. 2020;14(5):371-380.
Steptoe A, Kivimäki M. Stress and cardiovascular disease. Nat Rev Cardiol. 2012 ;9(6):360-370.
Knight EL, Jiang Y, Rodriguez-Stanley J, Almeida DM, Engeland CG, Zilioli S. Perceived stress is linked to heightened biomarkers of inflammation via diurnal cortisol in a national sample of adults. Brain Behav Immun. 2021;93:206-213.
Gianferante D, Thoma M V, Hanlin L, et al. Post-stress rumination predicts HPA axis responses to repeated acute stress. Psychoneuroendocrinology. 2014 ;49:244-252.
Young ES, Doom JR, Farrell AK, et al. Life stress and cortisol reactivity: An exploratory analysis of the effects of stress exposure across life on HPA-axis functioning. Dev Psychopathol. 2021;33(1):301-312.
Sterling P, Eyer J. Allostasis: a new paradigm to explain arousal pathology. En: Fisher S y Reason J, editor. Handbook of Life Stress, Cognition and Health. Philadelphia: John Wiley & Sons 1988: 629-639.
Sandner M, Lois G, Streit F, et al. Investigating individual stress reactivity: High hair cortisol predicts lower acute stress responses. Psychoneuroendocrinology. 2020;118: 1-10
Obasi EM, Shirtcliff EA, Cavanagh L, Ratliff KL, Pittman DM, Brooks JJ. Hypothalamic-Pituitary-Adrenal eeactivity to acute stress: an investigation into the roles of perceived stress and family resources. Prev Sci. 2017;18(8):923-931.
Lupien SJ, McEwen BS, Gunnar MR, Heim C. Effects of stress throughout the lifespan on the brain, behaviour and cognition. Nat Rev Neurosci. 2009;10(6):434-445.
Gunnar M, Quevedo K. The neurobiology of stress and development. Annu Rev Psychol. 2007;58:145-173.
Dmitrieva NO, Almeida DM, Dmitrieva J, Loken E, Pieper CF. A day-centered approach to modeling cortisol: Diurnal cortisol profiles and their associations among U.S. adults. Psychoneuroendocrinology. 2013;38(10):2354-2365.
Ostberg O, Horne JA. A Self Assessment Questionnaire to Determine Morningness Eveningness in Human Circadian Rhythms. Int J Chronobiol. 1976;4(2):97-110.
De Punder K, Heim C, Entringer S. Association between chronotype and body mass index: The role of C-reactive protein and the cortisol response to stress. Psychoneuroendocrinology. 2019;109: 1-7.
Åkerstedt T, Fröberg JE. Interindividual differences in circadian patterns of catecholamine excretion, body temperature, performance, and subjective arousal. Biol Psychol. 1976 4(4):277-292.
Lavalle-González FJ, Zacarías Villarreal-Pérez J, González-González G, et al. Validación de la medición de cortisol en saliva de una población de adultos jóvenes. Rev Endocrinol Nutr. 2011;19(4):146-148.
Hostinar CE, McQuillan MT, Mirous HJ, Grant KE, Adam EK. Cortisol responses to a group public speaking task for adolescents: Variations by age, gender, and race. Psychoneuroendocrinology. 2014;50:155
Guo J, Mrug S, Knight DC. Emotion socialization as a predictor of physiological and psychological responses to stress. Physiol Behav. 2017 1;175:119-129.
Roos LE, Giuliano RJ, Beauchamp KG, Gunnar M, Amidon B, Fisher PA. Validation of autonomic and endocrine reactivity to a laboratory stressor in young children. Psychoneuroendocrinology. 2017;77:51-55.
Mezzullo M, Fanelli F, Di Dalmazi Get al. Salivary cortisol and cortisone responses to short-term psychological stress challenge in late adolescent and young women with different hyperandrogenic states. Psychoneuroendocrinology. 2018;91:31-40.
Wadsworth ME, Broderick A V, Loughlin-Presnal JE, et al. Co-activation of SAM and HPA responses to acute stress: A review of the literature and test of differential associations with preadolescents’ internalizing and externalizing. Psychobiol. 2019;61(7):1079-1093.
Kimura K, Izawa S, Sugaya N, et al. The biological effects of acute psychosocial stress on delay discounting. Psychoneuroendocrinology. 2013;38(10):2300–2308.
McInnis CM, Thoma M V, Gianferante D, et al. Measures of adiposity predict interleukin-6 responses to repeated psychosocial stress. Brain Behav Immun. 2014 1;42:33–40.
Thoma M V., Gianferante D, Hanlin L, Fiksdal A, Chen X, Rohleder N. Stronger hypothalamus-pituitary-adrenal axis habituation predicts lesser sensitization of inflammatory response to repeated acute stress exposures in healthy young adults. Brain Behav Immun. 2017 1;61:228–235.
Manigault AW, Zoccola PM, Wüst S, Yim IS. Corroborative evidence for an association between initial hypothalamic-pituitary-adrenocortical axis reactivity and subsequent habituation in humans. Psychoneuroendocrinology. 2020 1;121:1-8.
Herbison CE, Henley D, Marsh J, et al. Characterization and novel analyses of acute stress response patterns in a population-based cohort of young adults: Influence of gender, smoking, and BMI. Stress. 2016 3;19(2):139–150.
Fiksdal A, Hanlin L, Kuras Y, et al. Associations between symptoms of depression and anxiety and cortisol responses to and recovery from acute stress. Psychoneuroendocrinology. 2019 1;102:44–52.
Finke JB, Behrje A, Heßlenberg E, Klucken T, Schächinger H. Stressed in afterthought: Neuroendocrine effects of social self-threat during physical effort are counteracted by performance feedback after stress exposure. Psychoneuroendocrinology. 2022 1;139:1-9.
Henze GI, Zänkert S, Urschler DF, et al. Testing the ecological validity of the Trier Social Stress Test: Association with real-life exam stress. Psychoneuroendocrinology. 2017 1;75:52–55.
Plieger T, Felten A, Diks E, Tepel J, Mies M, Reuter M. The impact of acute stress on cognitive functioning: a matter of cognitive demands? Cogn Neuropsychiatry. 2017 2;22(1):69–82.
Manigault AW, Shorey RC, Appelmann H, et al. Gender roles are related to cortisol habituation to repeated social evaluative stressors in adults: secondary analyses from a randomized controlled trial. Stress. 2021;24(6):723–733.
Lam JCW, Shields GS, Trainor BC, Slavich GM, Yonelinas AP. Greater lifetime stress exposure predicts blunted cortisol but heightened DHEA responses to acute stress. Stress and Health. 2019 1;35(1):15–26.
Hauck F, Romero Gibu L, Jansen S, Rohleder N. Differences in acute stress responses depending on first or second language in a Hispanic-American sample. Stress. 2022;25(1):313–322.
Hidalgo V, Villada C, Almela M, Espn L, Gmez-Amor J, Salvador A. Enhancing effects of acute psychosocial stress on priming of non-declarative memory in healthy young adults. Stress. 2012;15(3):329–338.
Sep MSC, Van Ast VA, Gorter R, Joëls M, Geuze E. Time-dependent effects of psychosocial stress on the contextualization of neutral memories. Psychoneuroendocrinology. 2019 1;108:140–149.
Kirschbaum C, Pirke KM, Hellhammer DH. The ‘Trier Social Stress Test’–a tool for investigating psychobiological stress responses in a laboratory setting. Neuropsychobiology. 1993;28(1-2):76-81.
Schwabe L, Haddad L, Schachinger H. HPA axis activation by a socially evaluated cold-pressor test. Psychoneuroendocrinology. 2008;33(6):890–895.
Smeets T, Cornelisse S, Quaedflieg CWEM, Meyer T, Jelicic M, Merckelbach H. Introducing the Maastricht Acute Stress Test (MAST): A quick and non-invasive approach to elicit robust autonomic and glucocorticoid stress responses. Psychoneuroendocrinology. 2012;37(12):1998–2008.
Richardson AE, VanderKaay Tomasulo MM. Stress-induced HPA activation in virtual navigation and spatial attention performance. BMC Neurosci. 2022 1;23(1):40:1-13.
Kühnel A, Kroemer NB, Elbau IG, , et al. Psychosocial stress reactivity habituates following acute physiological stress. Hum Brain Mapp. 2020 1;41(14):4010–4023.
Dalile B, La Torre D, Verbeke K, Va Oudenhove L, Vervliet B. When the mind says one thing, but the HPA axis says another: Lack of coherence between subjective and neuroendocrine stress response trajectories in healthy men. Psychoneuroendocrinology. 2022 1;139:1-10.
VanBruggen MD, Hackney AC, McMurray RG, Ondrak KS. The relationship between serum and salivary cortisol levels in response to different intensities of exercise. Int J Sports Physiol Perform. 2011;6(3):396–407.
Vanaelst B, Huybrechts I, Bammann K, et al. Intercorrelations between serum, salivary, and hair cortisol and child-reported estimates of stress in elementary school girls. Psychophysiology. 2012;49(8):1072–1081.

Barrientos Moral, Laura
Odontólogo Universidad Alfonso X El Sabio (UAX). Máster en Cirugía Oral, Implantes y Periodoncia (UAX). Profesora de Periodoncia en Grado de Odontología (UAX). Doctorando en la Universidad de Alcalá de Henares (UAH).
Paz Cortés, Marta Macarena
Odontopediatra. Especialista en niño con necesidades especiales UCM. Doctora en Odontología UCM. Coordinadora de Odontopediatría en el Grado de Odontología UAX. Profesora del Máster de Odontopediatría UCM y UAX.
Martín Vacas, Andrea
Odontopediatra. Especialista en el niño con necesidades especiales Universidad Complutense de Madrid (UCM). Doctora en Odontología UCM. Profesora de Odontopediatría en el Grado de Odontología UAX. Profesora del Master de Odontopediatría UCM y UAX.
Aragoneses Lamas, Juan Manuel
Decano de la Facultad de Odontología UAX.
Indexada en / Indexed in: – IME – IBECS – LATINDEX – GOOGLE ACADÉMICO.
Correspondencia: Laura Barrientos Moral. Avenida Universidad, 1, 28691. Villanueva de la Cañada, Madrid. [email protected] / [email protected].