CASO CLÍNICO
Grano de Oro Cordero EC, Galán Hernández RJ. Enfoque conservador en paciente con múltiples lesiones periapicales radiolúcidas: abordaje combinado endodóntico-quirúrgico. Cient. Dent. 2020; 17; 3; 15-21
Enfoque conservador en paciente con múltiples lesiones periapicales radiolúcidas: Abordaje combinado endodóntico-quirúrgico
Se presenta el caso de un paciente varón de 43 años con lesiones periapicales radiolúcidas de origen endodóntico en dientes pilares de rehabilitación fija metalocerámica, que acude a consulta para valorar la posibilidad de mantener sus dientes.
Tras la exploración clínica y radiológica mediante radiografías periapicales y tomografía computerizada de haz cónico (CBCT) se decide realizar un abordaje combinado endodóntico-quirúrgico.
La evolución clínica fue favorable y los controles radiográficos y tomográficos mostraron la resolución de las lesiones radiolúcidas preexistentes.
El retratamiento endodóntico combinado con la microcirugía periapical son herramientas eficaces en el tratamiento conservador de dientes con lesiones periapicales de origen endodóntico.
In this case report, we present a 43- year old male patient with multiple periapical radiolucent lesions caused by endodontic failure in teeth supporting a metalloceramic prosthetic rehabilitation, who came to the office asking for any possibility to maintain his teeth.
After clinical and radiological exploration with periapical x-rays and cone beam computer tomography (CBCT), we decided to use a combined endodonticsurgical approach.
Clinical evolution was favourable, and radiologica – tomographic controls showed complete healing of periapical radiolucent lesions.
Endodontic retreatment combined with periapical microsurgery are effective tools for conservative treatment in teeth with periapical lesions caused by endodontic failures.
Paciente varón de 43 años, sin antecedentes médicos de interés, portador de rehabilitación protética mediante pernos intrarradiculares y coronas metalocerámicas de 16 a 26 que acude a consulta por infecciones de repetición y fístulas en sector anterosuperior y zona 25-26. El paciente desea valorar la posibilidad de mantener sus dientes, ya que el tratamiento que le han propuesto consiste en la extracción de todos ellos y colocación de implantes.
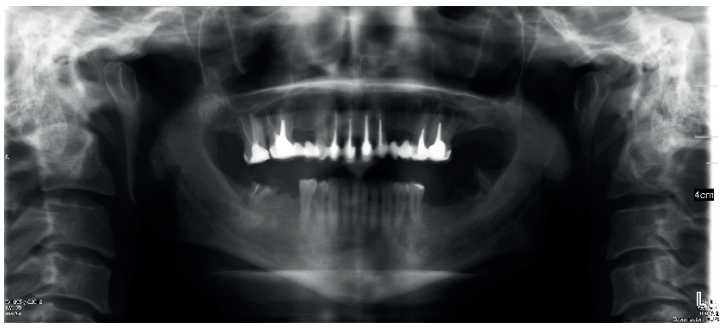
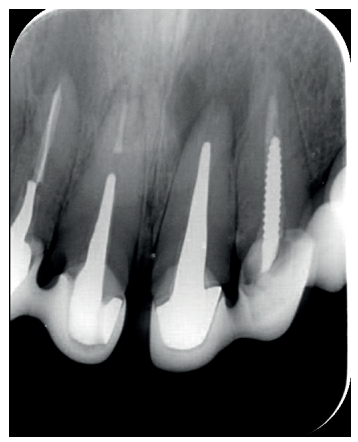
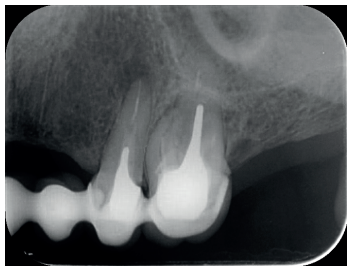
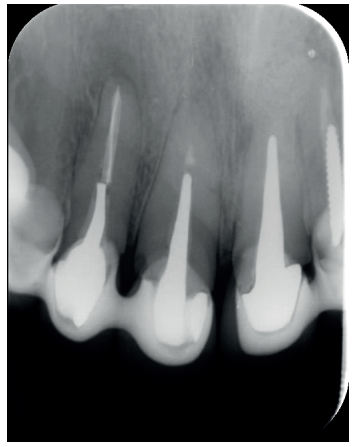
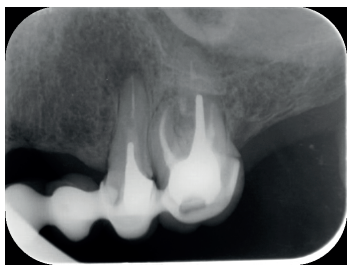
El paciente aporta como estudio radiológico una ortopantomografía (OPG), (Figura 1). Se realizaron radiografías periapicales (Figuras 2 y 3), así como exploración clínica incluyendo la valoración periodontal de los dientes afectados, sin observar profundidades de sondaje aumentadas que pudieran indicar la existencia de lesiones endoperiodontales.
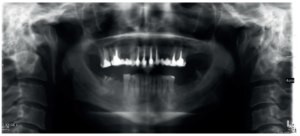
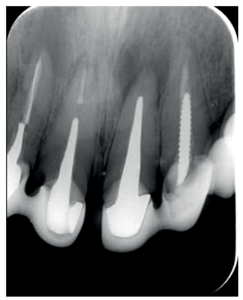
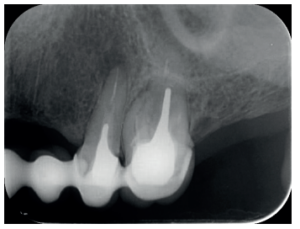
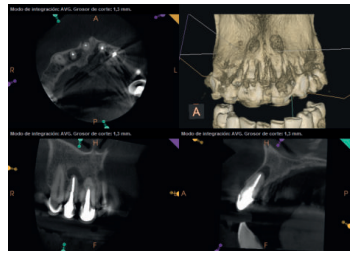
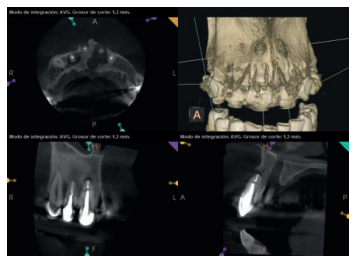
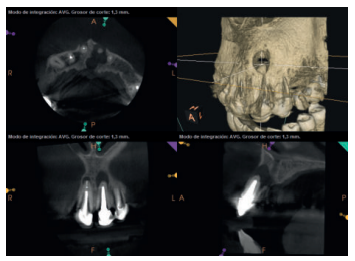
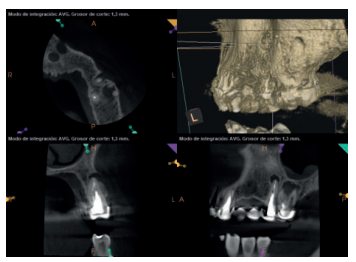
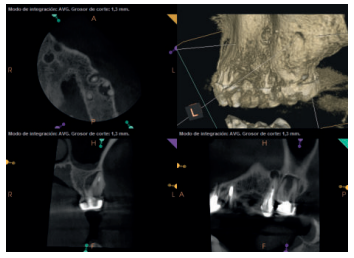
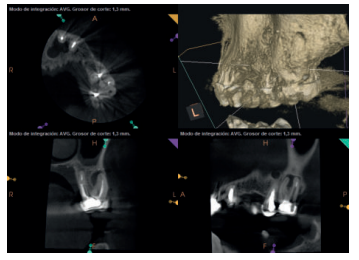
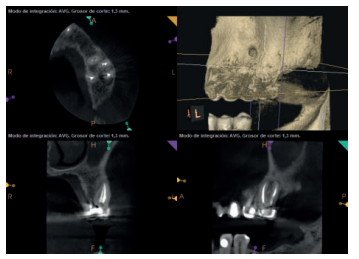
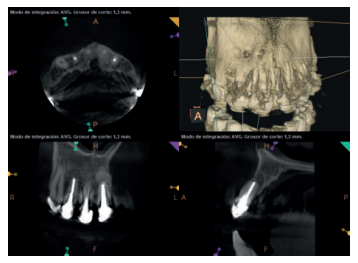
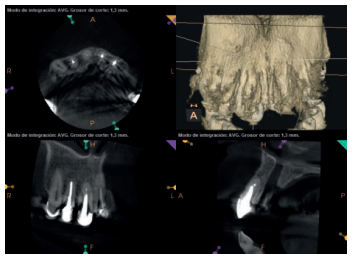
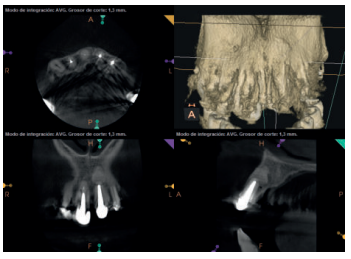
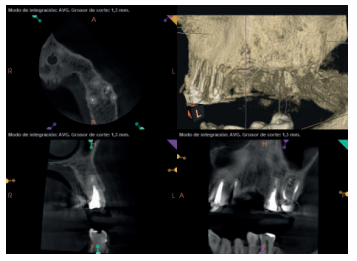
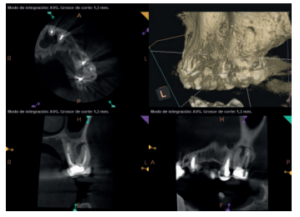
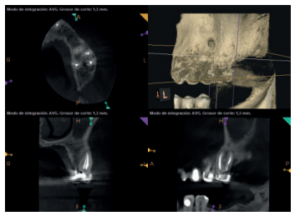
Para confirmar el origen endodóntico y el tamaño de las lesiones se realizaron exploraciones tomográficas con espesor de corte de 75 micras mediante CBCT CS8100 (Carestream Dental® ) en las que se evidenciaron lesiones periapicales radiolúcidas a nivel de 12, 11, 21 (con afectación bicortical), 25 y raíces vestibulares de 26 (Figuras 4 a 8).
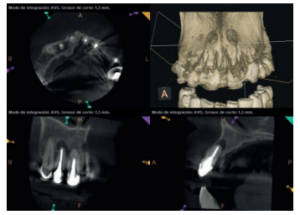
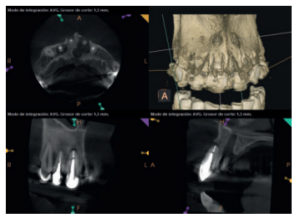
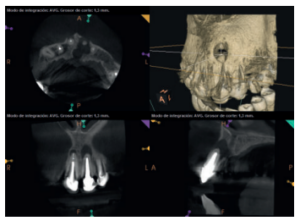
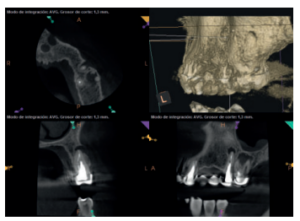
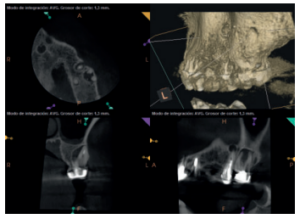
Se informó al paciente sobre la situación de sus dientes, obteniendo su consentimiento para realizar microcirugía apical a nivel de los tres incisivos superiores (12, 11 y 21), así como la necesidad de utilizar técnicas de regeneración ósea guiada (ROG) en 21.
Por otra parte, las raíces vestibulares del 26 presentaban un tratamiento de conductos claramente deficiente, con subextensión de varios milímetros, así como conducto mesiopalatino (MP) omitido; por lo que se planteó al paciente la necesidad de reendodonciar dichas raíces, antes de realizar la microcirugía del 25 (Figura 9).
Se realizó microcirugía periapical bajo magnificación mediante microscopio operatorio (KapsTM) a nivel de los incisivos superiores. Se consiguió el acceso a las lesiones apicales tras incisión de Neumann modificada. Una vez eliminadas dichas lesiones mediante cucharillas de legrado y curetas se realizaron apicectomías eliminando los últimos 3 mm de cada raíz, retrocavidades de 3 mm de profundidad mediante ultrasonidos (Newtronc , Satelec) y obturación mediante cemento biocerámico (Biodentine® , Septodont). En 21 además, se colocó membrana de colágeno (Bioguide® , Geistlich) en fondo palatino y se rellenó el defecto con matriz ósea porosa de origen bovino (BioOss® , Geistlich) antes de colocar una nueva membrana de colágeno por vestibular y suturar el colgajo mediante puntos simples con monofilamento de Poliamida 5/0 (Supramid® , Braun).
Posteriormente se realizó el retratamiento de conductos de las raíces vestibulares del 26, practicando un acceso coronal a través de la corona, eliminando parte del muñón colado, localizando el conducto MP omitido y desobturando los conductos mesiovestibular (MV) y distovestibular (DV). Una vez desinfectados y conformados dichos conductos se obturaron mediante cemento sellador biocerámico (BioRoot RCSTM, Septodont) y gutapercha.
A los seis meses el paciente acudió a revisión sin ninguna sintomatología, tanto a nivel anterior como posterior. En las radiografías periapicales se apreció una disminución en el tamaño de las lesiones periapicales radiolúcidas preexistentes (Figuras 10 y 11). Dado que faltaba tratar la lesión del 25, se realizó CBCT de control donde se comprobó la mejoría a nivel del 26 (Figura 12), por lo que se programó la microcirugía del 25.
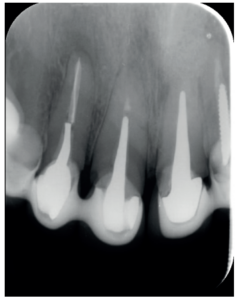
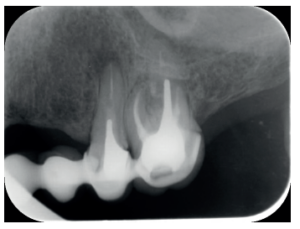
prexistente.
Una vez realizada la microcirugía del 25, el paciente no volvió a presentar ninguna sintomatología y las tomografías de control a 12 meses (en 25) y a 18 meses en los dientes restantes mostraron la regeneración de las lesiones periapicales radiolúcidas preexistentes en todos los dientes tratados (Figuras 13 a 16).
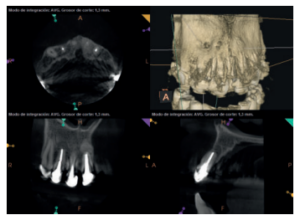
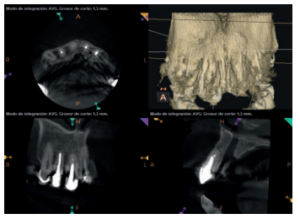
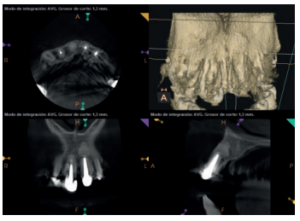
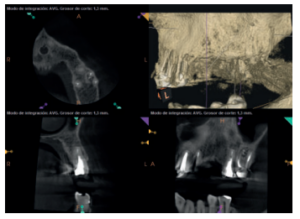
Para el correcto diagnóstico de lesiones radiolúcidas a nivel periapical es importante disponer de imágenes radiológicas que muestren con precisión la situación y tamaño de dichas lesiones. En nuestro caso el paciente aportaba una ortopantomografía. Este tipo de radiografía no es adecuada para el diagnóstico en endodoncia. La radiografía periapical aporta mejor definición, especialmente a nivel anterior, ya que presenta una menor distorsión. Actualmente el CBCT es la prueba radiológica más fiable, ya que proporciona imágenes en las tres dimensiones del espacio, lo que permite diagnósticos más precisos1,2 .
Ante los fracasos en dientes con múltiples tratamientos previos, como en el caso descrito, es importante afrontar el diagnóstico desde un punto de vista multidisciplinar. La exploración periodontal mediante sondaje es fundamental para conocer el estado periodontal y descartar la presencia de lesiones endoperiodontales de origen periodontal, así como de fracturas verticales3 .
Las opciones terapéuticas conservadoras ante los fracasos de origen endodóntico son el retratamiento de conductos no quirúrgico y la cirugía periapical. Diversos estudios muestran tasas de éxito similares (en torno al 75%) en ambos tratamientos, por lo que la elección entre uno u otro debe basarse en otros aspectos, como la facilidad de acceso por vía coronal o la calidad de la obturación de los conductos radiculares del tratamiento endodóntico previo4,5 .
La presencia de postes intraconducto en los dientes unirradiculares de nuestro caso, cuya remoción hubiera supuesto el sacrificio del escaso diente remanente que pudiera quedar bajo las coronas metalocerámicas, hizo que nos decantásemos por la cirugía periapical en dichos dientes. Sin embargo, el 26 presentaba las raíces vestibulares varios milímetros subobturadas y además la CBCT mostraba la presencia de un conducto MP omitido, por lo que en este diente optamos por un retratamiento de conductos no quirúrgico.
Autores como Kim y cols. destacan la importancia de algunos aspectos de la técnica quirúrgica actual con respecto a la cirugía periapical tradicional, tales como la realización de apicectomías de 3 mm sin bisel, retropreparaciones apicales con ultrasonidos y obturación retrógrada con materiales biocerámicos; todo ello utilizando el microscopio operatorio que es la herramienta fundamental que ha permitido mejorar mucho el pronóstico de estos tratamientos6 .
Cuando realizamos tratamientos combinados endodóntico-quirúrgicos, uno de los factores a tener presente es la necesidad de aplicar, o no, técnicas combinadas de regeneración ósea guiada (ROG)7 .
Al igual que en otras reconstrucciones de defectos óseos máxilo-mandibulares debemos saber si el defecto es de tamaño crítico, o no crítico8,9. En los primeros no se va a producir regeneración espontánea por parte del paciente, mientras que en los segundos podrá esperarse la regeneración ósea del defecto si se dan las condiciones adecuadas.
Entre estas condiciones deben estar presentes:10
- Mantenimiento del volumen del defecto que deseamos regenerar.
- Presencia en el interior de este volumen de un coágulo estable, que permita la organización del mismo y la migración de células formadoras de hueso.
- Evitar la invasión de fibroblastos o tejidos blandos circundantes al área a regenerar.
Otra característica a tener en cuenta para determinar las posibilidades de regeneración del defecto óseo periapical es el número de paredes destruidas por el proceso infeccioso. No cabe esperar el mismo grado de recuperación espontánea ante defectos óseos de múltiples paredes11, a pesar de realizar un correcto sellado apical y la eliminación del tejido inflamatorio asociado.
En el caso que nos ocupa encontramos diferentes situaciones respecto a las lesiones periapicales, ya que las mismas afectan a múltiples dientes, con diferente anatomía, y distinto grado de éxito en el tratamiento aplicado con anterioridad.
En los dientes 12, 11 y 25 el defecto óseo presente es de pequeño tamaño (estimado en 0,2, 0,03 y 0,05 cm3 , respectivamente) con ausencia de una pared y que, tras el abordaje quirúrgico, ostectomía con fresado óseo del área apical y legrado, presentan una arquitectura favorable para la regeneración espontánea, por lo que la actitud más razonable fue no aportar biomateriales para intentar mejorar la regeneración ósea.
Por otro lado, la situación inicial de la pieza 21, con un defecto de 0,35 cm3 de dos paredes opuestas de espesor total vestíbulo-palatal, que llega al alcanzar el pedículo vásculo-nervioso nasopalatino sin solución de continuidad, nos hace plantear una estrategia distinta a la anterior.
En este tipo de defectos óseos tiende a colapsar con más facilidad la cavidad o espacio residual generado por el legrado del granuloma apical que los presentes a nivel de 12, 11 y 25, donde no existe la posibilidad de invasión de fibroblastos desde la vertiente palatina.
Por ello, tras realizar la apicectomía y el sellado apical de conductos con BiodentineTM (Septodont), aplicamos técnicas complementarias de ROG, para mantener dicho volumen utilizando membranas reabsorbibles de colágeno (Bio-Gide® , Geistlich) como mecanismo de contención a la invasión de los tejidos blandos en ambas vertientes vestibular y palatina, asociando el relleno de la cavidad con 0,5 gr de matriz ósea porosa de origen bovino (Bio-Oss® , Geistlich) con el fin de evitar el colapso de la membrana de colágeno y actuar como material osteoconductor12 .
Se realizaron controles radiológicos a los 6, 12 y 18 meses mediante CBCT, apreciándose ausencia de sintomatología y reversión del cuadro infeccioso crónico, así como progresividad y estabilidad en la regeneración ósea apical. A nivel del 21 se aprecia radioopacidad periapical, sin pérdida de volumen, y ausencia de invasión del espacio preservado por el tejido blando circundante. Si bien algunos autores han utilizado plasma rico en factores de crecimiento (PRGF) asociado a Bio-Oss® y Bio-Gide® en casos similares al nuestro, hemos obtenido un resultado adecuado sin aplicar PRGF como técnica complementaria13.
Respecto al resto de lesiones periapicales, debido a su tamaño presentaron una regeneración espontánea favorable, constatando que no es preciso realizar ROG en lesiones de pequeño tamaño que no presentan defecto en túnel, al igual que opinan otros autores7,14 .
- El retratamiento endodóntico combinado con la microcirugía periapical son herramientas eficaces en el tratamiento conservador de lesiones periapicales de origen endodóntico.
- El diagnóstico multidisciplinar es fundamental para determinar el tratamiento más adecuado en cada caso.
Los avances diagnósticos y terapéuticos en el campo de la endodoncia y de la cirugía periapical permiten un abordaje conservador de las lesiones de origen endodóntico, permitiendo mantener dientes y recuperar el hueso perdido como consecuencia de dichas lesiones.
Ee J, Fayad MI, Johnson BR. Comparison of Endodontic Diagnosis and Treatment Planning Decisions Using Cone-beam Volumetric Tomography Versus Periapical Radiography. J Endod 2014;40(7):910–6.
Mota de Almeida FJ, Knutsson K, Flygare L. The impact of cone beam computed tomography on the choice of endodontic diagnosis. Int Endod J 2015;48(6):564–72.
Tsesis I, Rosen E, Tamse A, Taschieri S, Kfir A. Diagnosis of vertical root fractures in endodontically treated teeth based on clinical and radiographic indices: a systematic review. J Endod 2010;36(9):1455–8.
Torabinejad M, Corr R, Handysides R, Shabahang S. Outcomes of nonsurgical retreatment and endodontic surgery: a systematic review. J Endod 2009;35(7):930–7.
Arx von T, Peñarrocha M, Jensen S. Prognostic factors in apical surgery with root-end filling: a meta-analysis. J Endod 2010;36(6):957–73.
Kim S, Kratchman S. Modern endodontic surgery concepts and practice: a review. J Endod 2006;32(7):601–23.
Tsesis I, Rosen E, Tamse A, Taschieri S, Del Fabbro M. Effect of guided tissue regeneration on the outcome of surgical endodontic treatment: a systematic review and meta-analysis. J Endod 2011;37(8):1039–45.
Schmitz JP, Hollinger JO. The critical size defect as an experimental model for craniomandibulofacial nonunions. Clin Orthop Relat Res 1986;205:299-308.
Hollinger JO, Kleinschmidt JC. The critical size defect as an experimental model to test bone repair materials. J Craniofac Surg 1990;1(1):60–8.
Schenk RK, Buser D, Hardwick WR, Dahlin C. Healing pattern of bone regeneration in membrane-protected defects: a histologic study in the canine mandible. Int J Oral Maxillofac Implants 1994;9(1):13–29.
Goldman HM, Cohen DW. The Infrabony Pocket: Classification and Treatment. J Periodontol 1958;29(4):272–91.
Chiapasco M, Rossi A, Motta JJ, Crescentini M. Spontaneous bone regeneration after enucleation of large mandibular cysts: a radiographic computed analysis of 27 consecutive cases. YJOMS 2000;58(9):942-9.
Taschieri S, Rosano G, Weinstein T, Bortolin M, Del Fabbro M. Treatment of through-and-through bone lesion using autologous growth factors and xenogeneic bone graft: a case report. Oral Maxillofac Surg 2012;16(1):57–64.
Ochandiano Caicoya S. Relleno de cavidades óseas en cirugía maxilofacial con materiales aloplásticos. Rev Esp Cir Oral Maxilofac 2007; 29(1):21-32.

Grano de Oro Cordero, Eugenio C.
Licenciado en Odontología. Especialista Universitario en Endodoncia. Práctica privada en Madrid.
Galán Hernández, Ramón J.
Doctor en Medicina y Cirugía, Especialista en Cirugía Oral y Maxilofacial. Hospital General Universitario Ciudad Real. Práctica privada en Ciudad Real y en Madrid.