Caso clínico
Sahli D, Revuelta Cortés P, Martínez Rodríguez N, Madrigal Martínez-Pereda C, Martínez-González JM.
Displasia cemento-ósea fl orida: caso clínico y revisión de la literatura. Cient. Dent. 2025; 22; 2; 42-49.
Displasia cemento-ósea florida: caso clínico y revisión de la literatura
Introducción
La displasia cemento-ósea (DCO) es una lesión fibro-ósea benigna caracterizada por la sustitución de hueso por tejido fibroso y material calcificado. Se clasifica en cuatro subtipos: periapical, focal, florida y florida familiar. Generalmente asintomática, su diagnóstico se basa en hallazgos clínicos y radiográficos, evitando procedimientos invasivos por el riesgo de complicaciones. El objetivo de este trabajo fue reportar la evolución de un caso de displasia cemento-ósea florida (DCOF), analizando el enfoque terapéutico y la evolución de esta entidad.
Métodos
Se presenta el caso clínico de una mujer caucásica de 47 años diagnosticada con DCOF, aportando radiografías realizadas entre 2018 y 2024 que evidenciaron una evolución típica de la enfermedad. La paciente sufrió una fractura vertical en el 36, que requirió extracción quirúrgica, analizando el tratamiento y posibles complicaciones.
Resultados
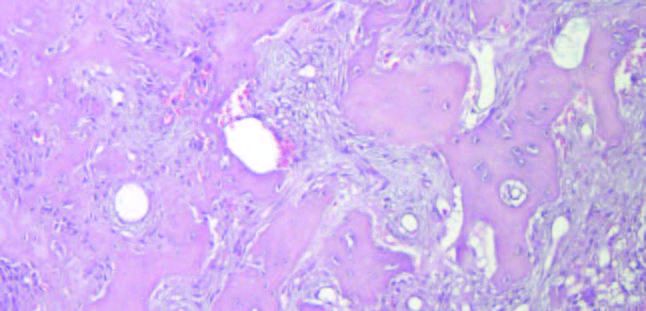
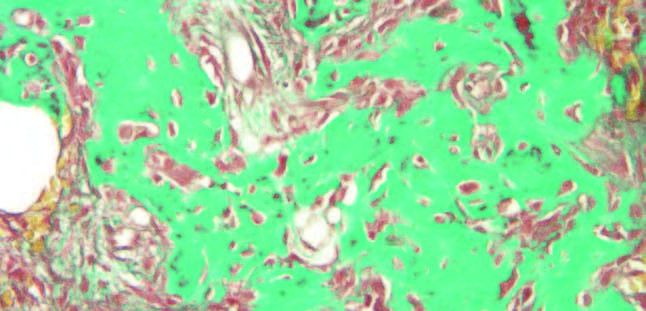
El análisis histopatológico, mostró una lesión fibro-ósea constituida por tejido conectivo fibroso con abundante celularidad fusiforme que rodea fragmentos trabeculares de tejido cemento-óseo vital, confirmando el diagnóstico de DCOF.
El manejo de esta patología suele ser conservador, salvo en casos sintomáticos o con complicaciones. La rehabilitación protésica, especialmente con implantes, representa un desafío debido a las alteraciones óseas y vasculares propias de la patología. La evidencia sugiere que los implantes tienen un mejor pronóstico en etapas avanzadas, cuando las lesiones muestran mayor grado de mineralización.
Conclusión
La DCOF suele manejarse sin intervenciones quirúrgicas debido a su naturaleza asintomática. Sin embargo, el seguimiento periódico es esencial para prevenir complicaciones y garantizar un manejo seguro, especialmente ante procedimientos dentales o rehabilitación con implantes.
Palabras clave: displasias, lesiones fibro-óseas, radiología, tratamiento.
Florid cemento-osseous dysplasia. Clinical case and review of the literature
Introduction
Cemento-osseous dysplasia (COD) is a benign fibro-osseous condition characterized by the replacement of normal bone with fibrous connective tissue and varying amounts of mineralized material. It is classified into four subtypes: periapical, focal, florid, and familial florid. COD is usually asymptomatic and is often discovered incidentally through routine radiographic examinations. Diagnosis relies on clinical and radiographic features, as invasive procedures are generally avoided due to the risk of complications. The aim of this paper is to present the progression of a case of Florid Cemento-Osseous Dysplasia (FCOD), evaluating the therapeutic approach and clinical evolution.
Methods
A 47-year-old Caucasian female was diagnosed with FCOD. Serial radiographs taken between 2018 and 2024 revealed a typical radiographic progression, with lesions transitioning from radiolucent to mixed and ultimately radiopaque areas. In 2024, the patient experienced a vertical fracture in tooth 36, requiring surgical extraction.
Results
Histopathological examination confirmed a fibro-osseous lesion composed of fibrous connective tissue with abundant spindle-shaped cells surrounding trabecular fragments of vital cemento-osseous material, consistent with FCOD. Management of this conditionis typically conservative unless symptoms or complications arise. Implant-based rehabilitation is challenging due to altered bone and vascular characteristics. However, studies suggest that implants may have better outcomes in advanced stages, when lesions are more mineralized.
Conclusion
FCOD is commonly managed without surgical intervention due to its asymptomatic nature. Nonetheless, regular monitoring is essential to prevent complications and ensure safe management, particularly when dental procedures or implant rehabilitation are considered.
Keywords: Dysplasias; Fibro-osseous lesions; Radiology; Treatment.
La displasia cemento-ósea (DCO) es una lesión fibro-ósea benigna del hueso que se caracteriza por la sustitución del hueso normal por tejido fibroso y, posteriormente, por su calcificación con material óseo y cementoso. Es generalmente asintomática y no requiere tratamiento1.
En el pasado la DCO se consideraba un proceso no neoplásico, idiopático, reactivo o hamartomatoso que surgía del periodonto debido a su estrecha asociación con los ápices de los dientes y su semejanza histológica con el cemento. Recientemente, se detectaron mutaciones patogénicas en la vía de señalización RAS-MAPK, con mutaciones de BRAF, HRAS, KRAS, NRAS y FGFR3 en la DCO2. Sin embargo, el mecanismo subyacente a la detención del crecimiento espontáneo que ocurre típicamente en la mayoría de las lesiones sigue siendo difícil de descifrar3.
La subclasificación de DCO se basa en su ubicación y extensión más que en el proceso histopatológico. Según la localización y la extensión de la afectación mandibular, las lesiones se pueden clasificar como DCO periapical, focal o florida.
En la displasia ósea periapical, los dientes anteriores inferiores suelen verse afectados. La displasia ósea focal se produce en una única zona de los dientes posteriores4.
La DCOF es una variante extensa de displasia ósea que se caracteriza por lesiones que afectan a dos o más cuadrantes de la mandíbula de forma bilateral y que, en algunos casos, también pueden comprometer los huesos maxilares5.
En 2022, la Organización Mundial de la Salud introdujo un cuarto subtipo en la clasificación de las DCO denominado displasia cemento-ósea florida familiar (DCOFF). Este subtipo se caracteriza por una aparición más temprana en comparación con la variante florida, a menudo afecta la erupción dental y tiende a provocar una expansión considerable del hueso mandibular4.
La presencia de DCO se detecta principalmente como un hallazgo accidental durante exámenes radiográficos6. Aunque, generalmente, se presenta de manera asintomática, puede volverse sintomática de forma espontánea o tras eventos como traumatismos, biopsias, extracciones dentales o tratamientos quirúrgicos en las áreas afectadas, debido a la introducción de bacterias en el hueso.
Por ello, la realización de biopsias y otras intervenciones quirúrgicas en regiones de DCO suelen considerarse contraindicadas. El diagnóstico, por lo tanto, se basa típicamente en la presentación clínica y radiográfica7- 12.
Aunque en la mayoría de los casos, la DCO es asintomática. Gabay y cols.7 en su revisión sistemática señalaron que la manifestación clínica más frecuente de la DCO sintomática era el dolor, seguido de inflamación en las áreas mandibulares afectadas y, con menor frecuencia, la presencia de infecciones en las regiones comprometidas por la lesión.
Radiográficamente, inicialmente se presenta como múltiples zonas radiotransparentes en las regiones periapicales, pero luego desarrolla un patrón radiomixto en las áreas afectadas. Con la maduración posterior, las lesiones se vuelven predominantemente radiodensas, pero a menudo tienen un borde radiotransparente.
La apariencia radiográfica de todas las formas de displasia ósea puede variar desde áreas hipodensas, pasando por mixtas, hasta hiperdensas debido a la maduración de la lesión con el tiempo y a la acumulación de tejido mineralizado8.
Inicialmente, la etapa radiotransparente puede ser mal diagnosticada como quistes radiculares o granulomas periapicales debido a su ubicación periapical. Sin embargo, la DCO generalmente se asocia a dientes vitales, no presenta síntomas clínicos y no requiere intervención9.
Las radiografías panorámicas e intraorales permiten un examen limitado de las estructuras anatómicas adyacentes. La tomografía computarizada de haz cónico (CBCT) permite una evaluación tridimensional (3D) de las estructuras anatómicas con una distorsión mínima y una alta resolución espacial, de ahí que resulte bastante beneficiosa para la detección de DCO10,11.
En cuanto al tratamiento, los pacientes asintomáticos deben ser controlados solo mediante exámenes clínicos y radiográficos a intervalos regulares semestrales.
Sin embargo, no existe un consenso final respecto al tratamiento de los pacientes sintomáticos, algunos autores sugieren terapia con antibióticos, mientras que otros como Gabay y cols. 7, propone intervenciones quirúrgicas.
El objetivo de este trabajo es reportar la evolución de un caso de DCOF, analizando el enfoque terapéutico y la evolución de esta entidad.
Mujer de 47 años que acudió derivada a la Unidad de Cirugía Bucal e Implantología de la Universidad Complutense de Madrid en 2021 para la valoración de lesiones radiomixtas presentes en múltiples localizaciones de la mandíbula. Como antecedentes médicos destacaba que la paciente padecía de una cardiopatía congénita cianótica, por lo cual fue sometida a una intervención quirúrgica de transposición vascular y que actualmente está tratada por un problema de insuficiencia cardíaca con bisoprolol (Laboratorios Normon S.A., Madrid, España) y sacubitril/valsartán (Entresto® Novartis Farmacéuticas S.A., Madrid, España).
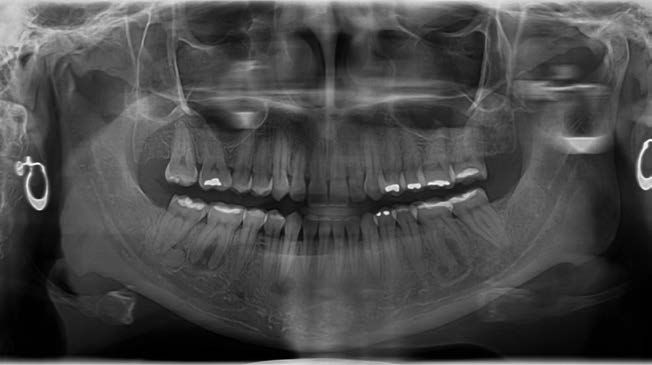
En una radiografía panorámica del año 2018 (Figura 1) se observaron lesiones difusas en la mandíbula, localizadas en las regiones periapicales de los dientes 36, 43, 46 y 47. Estas lesiones presentaban un predominio de áreas radiotransparentes, con la presencia de pequeñas zonas de material radiodenso.
En la radiografía panorámica de 2021 (Figura 2) se evidenciaba una progresión significativa de la lesión, caracterizada por un aumento en la aposición de material radiodenso, especialmente en el cuarto cuadrante. La paciente permanecía asintomática en el momento de la evaluación. Se estableció el diagnóstico de DCOF y se optó por una conducta terapéutica expectante, con controles periódicos cada 6 meses.
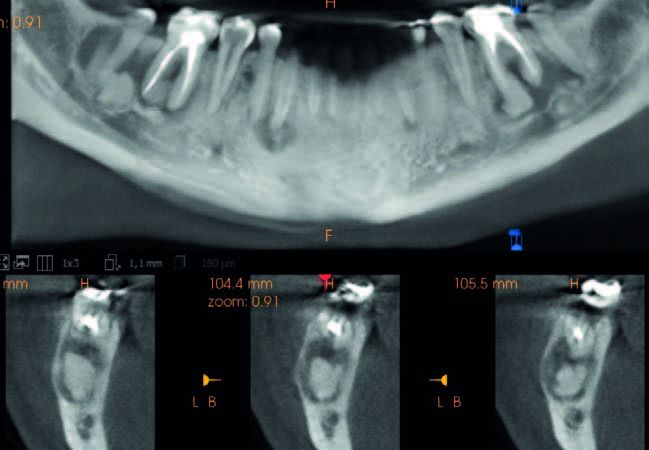
En 2023 se llevó a cabo una nueva evaluación radiográfica, complementada con un CBCT (Figura 3). En el estudio se identificaron áreas hiperdensas bien definidas, correspondientes a las regiones de los dientes 36, 43, 46 y 47. Estas áreas estaban rodeadas por un halo radiotransparente de forma irregular, sugiriendo la presencia de material mineralizado dentro de un tejido fibroso menos denso. Esas características radiográficas eran compatibles con un patrón intermedio de DCOF, que incluye la transición típica desde una fase predominantemente radiotransparente a una fase mixta.
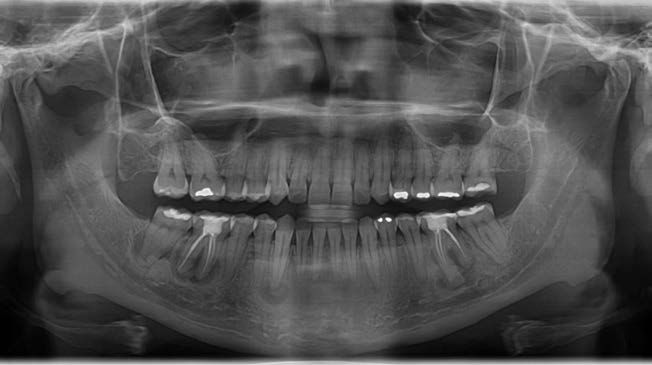
En noviembre de 2024, la paciente acudió a consulta presentando una fractura vertical en el molar 36, lo que requirió su exodoncia. A nivel radiográfico (Figura 4), se observó un aumento significativo de material radiodenso en la zona, particularmente en la región de la raíz mesial.
Se pautó una profilaxis antibiótica (2 gramos de amoxicilina 1 hora antes de la intervención). Se procedió a la realización de la cirugía, se realizó una técnica anestésica troncular para el bloqueo del nervio dentario inferior juntamente con el nervio lingual y el bloqueo del nervio bucal. Se realizó una incisión intrasulcular desde la cara distal del 37 hasta mesial del 34.
Posteriormente, se procedió a realizar la odontosección seguida de la luxación de las raíces. Sin embargo, se notó resistencia durante el procedimiento, por lo tanto, se llevó a cabo una ostectomía liberadora utilizando una fresa redonda de carburo de tungsteno montada en una pieza de mano. A continuación de continuó, con la luxación de las raíces y se procedió a su extracción sin complicaciones.
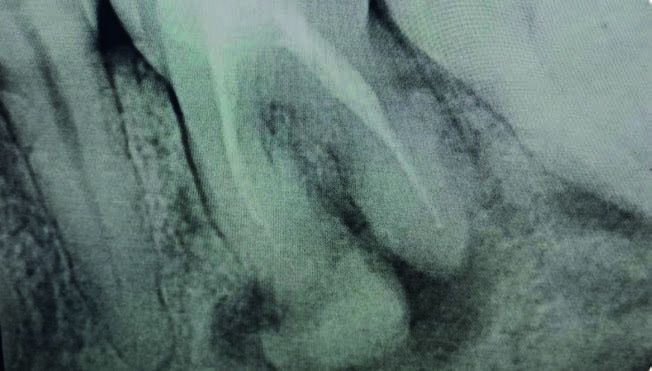
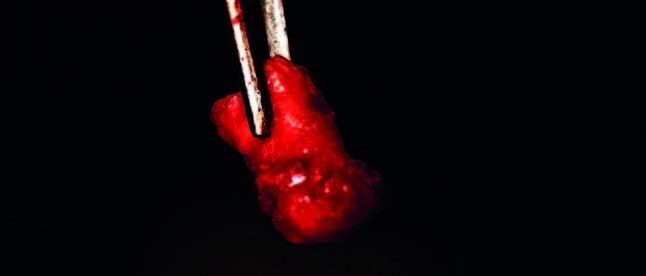
La raíz mesial presentaba un material adherido que tenía una consistencia heterogénea (Figura 5). En el fondo del alveolo, se observó tejido que se desprendía fácilmente, caracterizado por un material igualmente heterogéneo, consistente en tejido fibroso intercalado con zonas de mayor densidad, compatibles con una osificación parcial en desarrollo. Este material junto a las raíces se remitió para su análisis histopatológico.
Se procedió a la irrigación del alveolo con clorhexidina al 0.2% y posteriormente con suero fisiológico y se suturó el colgajo con seda de 4/0 (Silkam®).
El análisis mediante tinciones de Hematoxilina-Eosina y Tricrómico de Masson, mostró una lesión fibro-ósea constituida por tejido conectivo fibroso con abundante celularidad fusiforme que rodeaba fragmentos trabeculares de tejido cemento-óseo vital con aposición celular blástica externa y clástica multinuclear, lo que confirma el diagnóstico de DCOF (Figuras 6 y 7).
Transcurridos 10 días, se procedió a la retirada de la sutura, observando una buena cicatrización de los tejidos blandos. Se realizó control clínico al mes donde se observó una correcta cicatrización mucosa.
El término DCOF fue sugerido por primera vez por Melrose y cols.12 en 1976 para describir una condición extensa de masas exuberantes de cemento y/o hueso que se observa en dos o más cuadrantes en ambas mandíbulas. La presentación más común es la afectación bilateral de la mandíbula con o sin afectación colateral del maxilar.
La DCOF es una lesión fibro-ósea reactiva no neoplásica confinada a las áreas alveolares de las mandíbulas. Más del 90% de los casos se han informado en mujeres negras de mediana edad6. No obstante, se pueden presentar en un amplio rango de edad (27-79 años) con una incidencia máxima en la cuarta o quinta década13,14.
Al comparar estos datos en otras poblaciones como las orientales y caucásicas, autores como Thakur y cols.12, y Decolibus y cols.2, señalan una afectación similar en la edad, pero no en la predilección del género.
Recientemente, en 2024 en una revisión sistemática realizada por Gabay y cols.7, reportaron que los 11 estudios mostraron que los pacientes de sexo femenino tenían una prevalencia más alta de desarrollar una DCOF que los pacientes de sexo masculino; datos que estarían en consonancia con el caso de la paciente que presentamos.
Pereira y cols.15 y Gabay y cols.7 informaron que el aumento de la edad se correlaciona con un mayor número de pacientes sintomáticos.. El dolor mandibular fue el síntoma de presentación más común en todos los casos sintomáticos diagnosticados histopatológicamente como osteomielitis en el contexto de la DCOF. La osteomielitis se ha atribuido a la maduración de la lesión, asociada con una producción progresiva de calcificación similar al cemento avascular. Esto aumenta la susceptibilidad de la lesión a las infecciones. Debido a su naturaleza avascular, la lesión puede no responder bien a la terapia con antibióticos, por lo que sería necesaria la eliminación del secuestro.
En cuanto a la localización, la literatura señala que la mandíbula, especialmente su región posterior, es la más frecuentemente afectada.
La DCOF generalmente es asintomática y la lesión puede pasar desapercibida durante varios años y, por lo tanto, a menudo se diagnostica por casualidad durante exámenes radiológicos de rutina13- 15.
Las radiografías panorámicas suelen ser suficientes para diagnosticar una DCO y sus subtipos. Sin embargo, para comprender la extensión de la lesión, el estadio de la enfermedad y la relación con las estructuras circundantes, se prefieren las exploraciones CBCT. Estas muestran imágenes tridimensionales de alta resolución para una representación precisa de la densidad de las lesiones, los estadios de maduración y las características10,15.
Las apariencias radiológicas pueden variar desde completamente radiotransparentes en las lesiones tempranas hasta radiodensas en las lesiones avanzadas. En la etapa intermedia , como refieren Alsufyani y cols.16, se presenta como lesiones radiomixtas.
En el presente caso clínico, en 2018 se observaron lesiones proliferativas e inmaduras con una apariencia radiotransparente. En etapas más avanzadas de maduración, se identificaron masas radiodensas en las radiografías panorámica realizadas en 2021 y 2023. Estas masas hiperdensas, localizadas en las regiones de los dientes 36, 46, 47 y 43, estaban rodeadas por un área hipodensa y adheridas a las raíces de los dientes correspondientes. Las lesiones estaban bien delineadas del hueso circundante. Muchos autores han informado la presencia de un borde radiotransparente circundante característico y distintivo en la DCO13.
En muchos casos, el diagnóstico de estas lesiones puede ser particularmente confuso porque las características radiográficas de las lesiones tempranas tienden a imitar las de un quiste periapical o granuloma. De manera similar, en la etapa radiomixta, la lesión podría confundirse con osteomielitis esclerosante crónica, fibroma cemento-osificante, odontoma y osteoblastoma6,17.
En fases avanzadas, con una notable mineralización, se puede plantear como diagnósticos diferenciales la displasia fibro-ósea, el fibroma osificante y el cementoma gigantiforme familiar12. Por tanto, los diagnósticos diferenciales varían según el estadio de maduración y abarcan lesiones fibro-óseas.
Durante el seguimiento realizado en nuestra Unidad de Cirugía Bucal e Implantología, se observó una evolución de las lesiones, pasando de un componente predominantemente fibroso a uno más mineralizado. Las características radiográficas de las lesiones, su extensión a lo largo de toda la mandíbula, junto con su evolución permitieron hacer un diagnóstico de presunción de DCOF, que más tarde fue confirmado mediante histopatología.
Histológicamente, todas las variantes de DCO tienen características microscópicas similares; un tejido mesenquimatoso de celularidad variable, compuesto por fibroblastos fusiformes, fibras colágenas y vasos sanguíneos, entremezclado con tejido mineralizado que consiste en osteoide, hueso reticulado y material similar al cemento, que se disponen en forma de trabéculas y osículos/cementículos irregulares y coalescentes. Durante la maduración, la matriz se fusiona para formar depósitos más grandes e hipocelulares con líneas de cemento irregulares. Es común encontrar hemorragia, especialmente cerca de la periferia, lo cual puede atribuirse a la fragilidad vascular en el tejido conectivo alterado presente en la DCO3,13.
La apariencia radiográfica de las lesiones suele mostrar correlación con las características histológicas. Los casos que presentan lesiones radiotransparentes con focos de opacificación o lesiones mixtas en la radiografía exhiben un tejido estromal abundante y celular, alta vascularidad y una cantidad baja a moderada de material mineralizado en forma de trabéculas cortas y curvilíneas. Por otro lado, las lesiones radiodensas disponen de una menor cantidad de tejido estromal con disminución de la celularidad, vascularidad mínima y láminas acelulares de material mineralizado13.
La paciente que se muestra en este trabajo estaba asintomática a lo largo de los años, sin embargo, presentó una fractura vertical en el diente 36 lo que hizo la extracción inevitable, solicitando posteriormente la colocación de un implante dental para la restauración protésica.
La literatura disponible sobre la rehabilitación con implantes en pacientes con DCO es escasa. En la actualidad, no existe uniformidad para esta forma de tratamiento, dado que la estructura ósea normal es reemplazada por fibroblastos y fibras de colágeno que incluyen cantidades variables de sustancias mineralizadas, teniendo como resultado una matriz ósea debilitada con una vascularización estromal subdesarrollada, con la consiguiente dificultad en el proceso de osteointegración18,19.
Hosseinpour y cols.20, en su revisión sistemática reportaron que la colocación de implantes en lesiones de DCO, en etapas tempranas o intermedias puede hacer fracasar la osteointegración debido a un contacto hueso implante restringido. Por el contrario, se ha demostrado que las lesiones de DCO en etapas tardías tienen un mayor porcentaje de tejido calcificado que las lesiones en etapas tempranas e intermedias, ya que la maduración de la lesión se caracteriza por la deposición gradual de componentes semejantes al cemento. Por consiguiente, si se indica terapia con implantes, estos deben insertarse únicamente en una lesión de DCO en etapas tardías con tejido calcificado fuertemente.
Li y cols.21 realizaron una revisión sistemática en la que compararon, entre otras, las complicaciones producidas entre los tratamientos con implantes versus tratamientos con prótesis removibles. Pudieron observar que en el caso de las rehabilitaciones implantológicas, los resultados son impredecibles aconsejando que estos se coloquen fuera de la zona displásica. Así mismo, en el caso de las rehabilitaciones con prótesis removibles, existe la posibilidad de exposición ósea con el consiguiente riesgo de infecciones.
En este sentido, Shadid y cols.22 reportaron una colocación exitosa de implantes con un seguimiento de 8 años en una mujer de 44 años que solicitó una restauración fija en la zona edéntula posterior mandibular, concluyendo que la rehabilitación con implantes en áreas edéntulas cercanas a lesiones de DCOF puede ser considerada, siempre y cuando se siga un estricto control de infecciones.
Al planificar la colocación de un implante en un paciente con DCO, hay que evitar el sobrecalentamiento durante la preparación del lecho receptor, asegurar una irrigación abundante para no causar un mayor daño al hueso, garantizar una integración y grosor óptimos del tejido blando periimplantario durante la fase de cicatrización, lograr un perfil de emergencia bien contorneado y restauraciones protésicas adecuadas, así como asegurar un mantenimiento regular y una correcta higiene oral por parte del paciente20,23.
En el caso de que se desarrolle una infección secundaria es probable que sea agresiva y difícil de tratar. Las principales complicaciones incluyen una mala cicatrización, un mayor riesgo de infección y fracturas mandibulares20.
Dado que no hay evidencia suficiente sobre el éxito a largo o incluso a corto plazo de la rehabilitación con implantes dentales en casos de DCO se recomiendan más estudios para comprobar viabilidad de esa modalidad de tratamiento20,22.
La DCOF, de carácter multifocal, suele manejarse sin intervenciones quirúrgicas debido a su naturaleza asintomática. Sin embargo, el seguimiento periódico es esencial para prevenir complicaciones y garantizar un manejo seguro, especialmente ante procedimientos dentales o rehabilitación con implantes.
Ravikumar SS, Vasupradha G, Menaka TR, Sankar SP. Focal cementoosseousdysplasia. J Oral Maxillofac Pathol. 2020;24(Suppl 1):S19-S22.2.
Decolibus K, Shahrabi-Farahani S, Brar A, Rasner SD, Aguirre SE, Owosho AA. Cemento-osseous dysplasia of the jaw: Demographic and clinical analysis of 191 new cases. Dent J (Basel).
2023;11(5):138.
Haefliger S, Turek D, Andrei V, et al. Cemento-osseous dysplasia is caused by RAS-MAPK activation. Pathology. 2023;55(3):324-328.
Nosé V, Lazar AJ. Update from the 5th edition of the World Health Organization classification of head and neck tumors: familial tumor syndromes. Head NeckPathol. 2022;16(1):143-157.
Farah CS, Matias MAT. Natural history of florid osseous dysplasia of the jaws with important clinical implications. Aust Endod J. 2021;47(3):684-689.
Salvi AS, Patankar S, Desai K, Wankhedkar D. Focal cemento-osseous dysplasia: A case report with a review of literature. J Oral Maxillofac Pathol. 2020;24(Suppl 1):S15-S18.
Gabay M, DiPede L, Fornatora M, Yang J, Ogwo C. Treatment indications for symptomatic versus asymptomatic florid cemento-osseous dysplasia in adult patients: a systematic review. Oral
Surg Oral Med Oral Pathol Oral Radiol. 2024;138(6):686-701.
Cavalcanti PHP, Nascimento EHL, Pontual MLDA, et al. Cemento-osseous dysplasias: imaging features based on cone beam computed tomography scans. Braz Dent J. 2018;29(1):99-104.
Günaçar DN, Köse TE, Arıcıoğlu B, Çene E. Retrospective radiological analysis of cemento-osseous dysplasia. Dent Med Probl. 2023;60(3):393-400.
Gumru B, Akkitap MP, Deveci S, Idman E. A retrospective cone beam computed tomography analysis of cemento-osseous dysplasia. J Dent Sci. 2021;16(4):1154-1161.
Park S, Jeon SJ, Yeom HG, Seo MS. Differential diagnosis of cementoosseous dysplasia and periapical cyst using texture analysis of CBCT. BMC Oral Health. 2024;24(1):442.
Thakur A, Gaikwad S, Tupkari JV, Ramaswami E. Florid cemento-osseous dysplasia: A case report. Indian J Dent Res. 2021;32(1):134.
Urs AB, Augustine J, Gupta S. Cementoosseous dysplasia: Clinicopathological spectrum of 10 cases analyzed in a tertiary dental institute. J Oral Maxillofac Pathol. 2020;24(3):576.
Grün P, Schneider B, Bandura P, Pfaffeneder-Mantai F, Bytyqi D, Turhani D. Bone remodelling after minimally invasive surgical management of a recurrent florid cemento-osseous dysplasia in a Caucasian woman – 18 years follow-up of a unique case. Int J Surg Case Rep. 2023;105:108074.
Pereira DL, Pires FR, Lopes MA, et al. Clinical, demographic, and radiographic analysis of 82 patients affected by florid osseous dysplasia: an international collaborative study. Oral Surg Oral Med Oral Pathol Oral Radiol. 2016;122(2):250-257.
Alsufyani NA, Lam EWN. Osseous (cemento-osseous) dysplasia of the jaws: clinical and radiographic analysis. J Can Dent Assoc. 2011;77:b70.
Aiuto R, Gucciardino F, Rapetti R, Siervo S, Bianch AE. Management of symptomatic florid cemento-osseous dysplasia: Literature review and case report. J Clin ExpDent. 2018;10(3):e291-5.
Aiuto R, Gucciardino F, Rapetti R, Siervo S, Bianch AE. Management of symptomatic florid cemento-osseous dysplasia: Literature review and case report. J Clin ExpDent. 2018;10(3):e291-5.
Jagtap R, Gupta S, Bhat M, Mehta N, Gupta S. Dilemma with implant placement in patients with florid cemento-osseous dysplasia: A literature review. Sci Prog. 2024;107(2):368504241244
Hosseinpour S, Khademi MH, Erfani M, Mosaddad SA, Heboyan A. Are implantbased treatments considered viable for patients with focal or florid cementoosseous dysplasia? A systematicreview.
Maxillofac Plast ReconstrSurg. 2024;46(1):23.
Li S, Delgado-Ruiz R, Romanos G. Dental implants versus removable prostheses for the management of edentulous sites in patients with florid cemento-osseous dysplasia: A systematic review of literature with a follow-up period of at least 3 years. Int J Oral Implantol Berl Ger. 2024;17(4):345- 56.
Shadid R, Kujan O. Success of dental implant osseointegration in a florid cemento-osseous dysplasia: A case report with 8-year follow-up. Clin Pract. 2020;10(3):1281.
Shin HS, Kim BC, Lim HJ, Jo SY, Lee J. Chronic osteomyelitis induced by the placement of dental implants on cemento-osseous dysplasia. Br J Oral Maxillofac Surg. 2019;57(3):268-270.

Sahli Dorsaf
Odontóloga. Alumna del Postgrado de Especialización en Cirugía Bucal e Implantología. Facultad de Odontología. Universidad Complutense de Madrid (UCM).
Revuelta Cortés, Pablo
Odontólogo. Alumno del Postgrado de Especialización en Cirugía Bucal e Implantología. Facultad de Odontología. Universidad Complutense de Madrid (UCM).
Martínez Rodríguez, Natalia
Doctora en Odontología. Profesora Asociada de Cirugía Bucal. Facultad de Odontología. Universidad Complutense de Madrid (UCM).
Madrigal Martínez-Pereda, Cristina
Codirectora del Postgrado de Especialización en Cirugía Bucal e Implantología. Profesora Contratada Doctor. Facultad de Odontología. Universidad Complutense de Madrid (UCM).
Martínez-González, José María
Profesor Titular Cirugía Maxilofacial. Facultad de Odontología. Universidad Complutense de Madrid (UCM).