Artículo original
Freire Mancebo Y, Larrosa Pérez M, Esteban Martínez I, Palma White B, Cisneros Cabello, R. Cementos de silicato de calcio: evaluación de la toxicidad y de la respuesta inflamatoria. Cient. Dent. 2021; 18; 3; 145-152
Cementos de silicato de calcio: evaluación de la toxicidad y de la respuesta inflamatoria
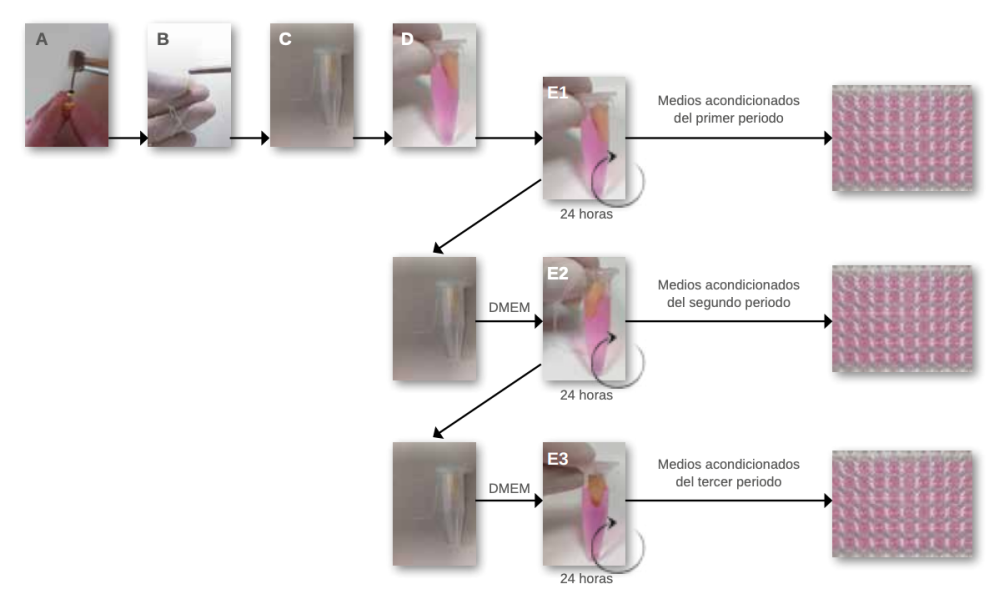
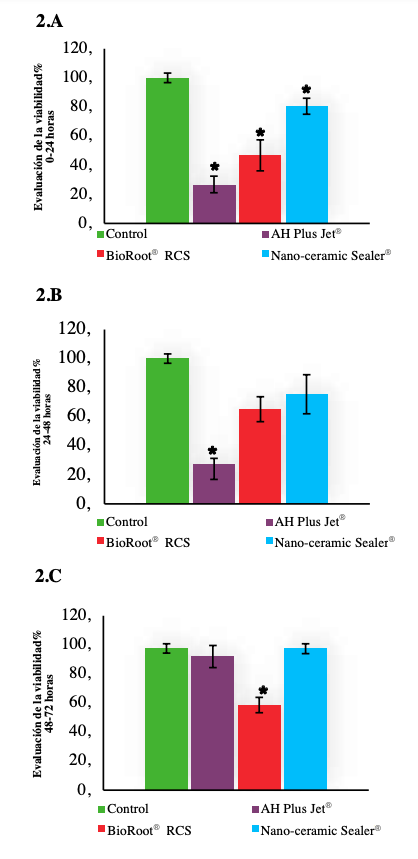
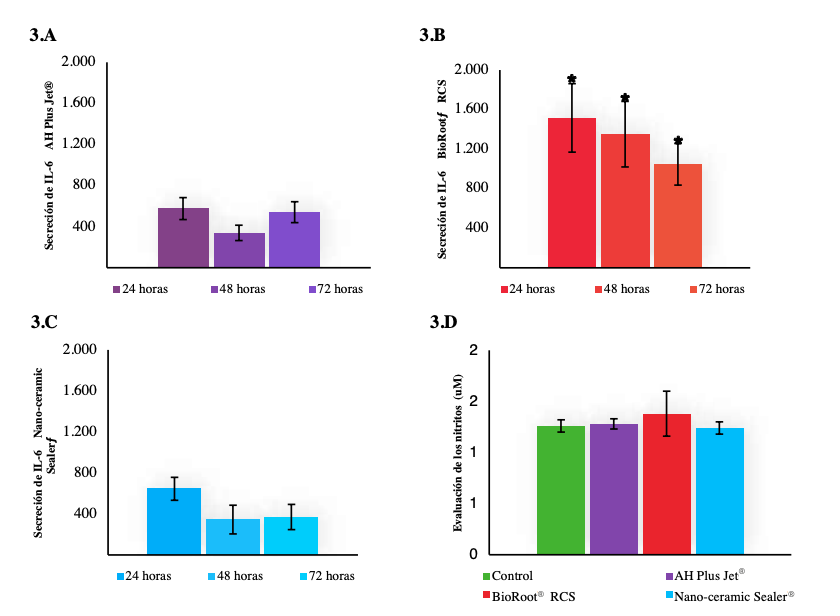
La biocompatibilidad de los cementos selladores es una característica que debe tenerse en cuenta, ya que podría influir en el resultado del tratamiento de conductos. El objetivo de este estudio fue analizar la citotoxicidad de los cementos selladores a base de silicatos BioRoot® RCS y Nano-ceramic Sealer®, y el sellador a base de resina epóxica AH Plus Jet®, así como su respuesta inflamatoria asociada en fibroblastos humanos. Se seleccionaron 36 dientes unirradiculares, se instrumentaron y obturaron con los selladores seleccionados. A continuación, se pusieron en contacto con el medio de cultivo para obtener los medios acondicionados a las 24, 48 y 72 horas. Los medios acondicionados obtenidos fueron cultivados con la línea celular de fibroblastos L-132. La viabilidad de las células se evaluó mediante el ensayo del bromuro de 3-(4,5-dimetiltiazol-2-il)-2,5 difenil tetrazolio (MTT). La respuesta inflamatoria se analizó mediante la medición de los niveles de IL-6 determinados a través del ensayo ELISA (ensayo por inmunoabsorción ligado a enzimas) y mediante los niveles de nitrito (ensayo de fluorescencia). Todos los selladores mostraron un cierto grado de citotoxicidad durante el tiempo de evaluación, mientras que sólo el BioRoot® RCS desencadenó una respuesta pro-inflamatoria. Es necesario seguir investigando para evaluar otros aspectos de la biocompatibilidad de los cementos selladores a base de silicato.
Biocompatibility of sealers is a feature to be taken into account as it might influence the outcome of the treatment. The aim of this study was to analyze the cytotoxicity of the silicate-based root canal sealers BioRoot™ RCS and Nanoceramic Sealer™and the epoxy-resin based sealer AH Plus Jet™, as well as their associated inflammatory response in human fibroblast. Thirty-six human teeth were selected, prepared, filled with the selected sealers and put in contact with culture medium to obtain extracts at 24, 48 and 72 hours. Then, the extracts were cultured with the L-132 fibroblast cell line. Cell viability was evaluated using the 3-(4,5-dimethylthiazol-2- yl)-2,5 diphenyl tetrazolium bromide (MTT) assay. Inflammatory response was analyzed by measuring IL-6 levels determined by ELISA and nitrite levels (fluorescence assay). All sealers showed a certain degree of cytotoxicity during the evaluation time, while only the BioRoot™ RCS triggered a pro-inflammatory response. Further research is needed to assess other aspects of biocompatibility of silicate-based root canal sealers.
En la actualidad, ninguno de los cementos de endodoncia presenta todas las características1 que un cemento ideal debería tener2 . Por lo tanto, los fabricantes tratan de mejorar constantemente estas propiedades, introduciendo nuevos cementos en el mercado3 . Dado que los cementos podrían llegar a los tejidos periodontales a través de las diferentes conexiones existentes, es importante conocer sus propiedades4 ya que podrían causar una respuesta5 . La biocompatibilidad es una de las características que podrían influir en el resultado del tratamiento endodóntico1 , y está determinada por diferentes aspectos, entre los que se incluye la citotoxicidad6 .
La citotoxicidad se define como la capacidad de un material para influir en la viabilidad celular7 y, en general, es el primer paso que se analiza al evaluar la biocompatibilidad8 . La Organización Internacional para la Normalización (ISO) sugiere la realización de ensayos de citotoxicidad “in vitro” al ser sencillos, controlables y reproducibles9 . Sin embargo, hay que tener en cuenta que la citotoxicidad sólo describe un aspecto de la biocompatibilidad7 . Otra posible respuesta, a los materiales potencialmente tóxicos, sería una reacción inflamatoria10. Se sabe que diferentes citoquinas proinflamatorias11, como la interleuquina (IL) y el factor de necrosis tumoral (TNF)12, participan en la respuesta inflamatoria contribuyendo al proceso de curación11.
Debido a las buenas propiedades de biocompatibilidad que presentan los cementos a base de silicato de calcio, recientemente se han desarrollado diferentes cementos selladores basados en dicho componente13-15, como el iRoot® SP, el BioRoot® RCS o el Nano-ceramic Sealer®. El BioRoot® RCS está compuesto por silicato tricálcico y polvo de óxido de circonio, que se mezcla con una solución acuosa a base de cloruro de calcio16,17, mientras que el cemento Nano-ceramic Sealer® está compuesto de silicatos de calcio, óxido de zirconio, agente espesante y rellenos15. Sin embargo, los cementos a base de resina epóxica se siguen utilizando de forma frecuente en los tratamientos de endodoncia18,19, siendo considerado el AH Plus® como el “gold standard”17,20,21.
El objetivo del presente estudio fue evaluar la citotoxicidad y la respuesta inflamatoria de los cementos a base de silicato de calcio Nano-ceramic Sealer® y el BioRoot® RCS, y compararlo con el cemento a base de resina AH Plus Jet®, en la línea celular de fibroblastos humanos L-132. Las hipótesis nulas planteadas establecieron que no se encontrarían diferencias entre los diferentes cementos, ni en términos de citotoxicidad ni en términos de respuesta inflamatoria.
Zhou HM, Du TF, Shen Y, Wang ZJ, Zheng YF, Haapasalo M. In vitro cytotoxicity of calcium silicate-containing endodontic sealers. J Endod 2015;41(1):56-61.
Lucena-Martín C, Ferrer-Luque CM, González-Rodríguez MP, RoblesGijón V, Navajas-Rodrguez MJM. A Comparative Study of Apical Leakage of Endomethasone, Top Seal, and Roeko Seal Sealer Cements. J Endod 2002;28(6):423-6.
Corral Nunez CM, Bosomworth HJ, Field C, Whitworth JM, Valentine RA. Biodentine and mineral trioxide aggregate induce similar cellular responses in a fibroblast cell line. J Endod 2014;40(3):406-11.
Huang TH, Lii CK, Chou MY, Kao CT. Lactate Dehydrogenase Leakage of Hepatocytes with AH26 and AH Plus Sealer Treatments. J Endod 2000;26(9):509-11.
Sousa CJ, Montes CR, Pascon EA, Loyola AM, Versiani MA. Comparison of the intraosseous biocompatibility of AH Plus, EndoREZ, and Epiphany root canal sealers. J Endod 2006;32(7):656-62.
Silva-Herzog D, Ramirez T, Mora J, Pozos AJ, Silva LA, Silva RA, et al. Preliminary study of the inflammatory response to subcutaneous implantation of three root canal sealers. Int Endod J 2011;44(5):440-6.
Peters OA. Research that matters – biocompatibility and cytotoxicity screening. Int Endod J 2013;46(3):195-7.
Tai KB, Huang FM, Chang YC. Cytotoxic Evaluation of Root Canal Filling Materials on Primary Human Oral Fibroblast Cultures and a Permanent Hamster Cell Line. J Endod 2001;27(9):571-3.
Scelza MZ, Linhares AB, da Silva LE, Granjeiro JM, Alves GG. A multiparametric assay to compare the cytotoxicity of endodontic sealers with primary human osteoblasts. Int Endod J 2012;45(1):12-8.
D. ÖM, Yilmaz S, Kalayci A, Zaimalu L. A comparison of the in vitro cytotoxicity of two root canal sealers. J Oral Rehabil 2003;30:426-9.
Chang SW, Lee SY, Kum KY, Kim EC. Effects of ProRoot MTA, Bioaggregate, and Micromega MTA on odontoblastic differentiation in human dental pulp cells. J Endod 2014;40(1):113-8.
Diomede F, Caputi S, Merciaro I, Frisone S, D’Arcangelo C, Piattelli A y cols. Proinflammatory cytokine release and cell growth inhibition in primary human oral cells after exposure to endodontic sealer. Int Endod J 2014;47(9):864-72.
Donnermeyer D, Bürklein S, Dammaschke T, Schäfer E. Endodontic sealers based on calcium silicates: a systematic review. Odontology 2018 2019;107(4):421-436.
Dimitrova-Nakov S, Uzunoglu E, Ardila-Osorio H, Baudry A, Richard G, Kellermann O y cols. In vitro bioactivity of Bioroot RCS, via A4 mouse pulpal stem cells. Dent Mater 2015;31(11):1290-7.
Collado-Gonzalez M, Garcia-Bernal D, Onate-Sanchez RE, Ortolani-Seltenerich PS, Lozano A, Forner L y cols. Biocompatibility of three new calcium silicate-based endodontic sealers on human periodontal ligament stem cells. Int Endod J 2017;50(9):875-84.
Khalil I, Naaman A, Camilleri J. Properties of Tricalcium Silicate Sealers. J Endod. 2016;42(10):1529-35.
Alsubait SA, Al Ajlan R, Mitwalli H, Aburaisi N, Mahmood A, Muthurangan M y cols. Cytotoxicity of Different Concentrations of Three Root Canal Sealers on Human Mesenchymal Stem Cells. Biomolecules. 2018;8(3). pii: E68
Ersahan S, Aydin C. Dislocation resistance of iRoot SP, a calcium silicatebased sealer, from radicular dentine. J Endod 2010;36(12):2000-2.
Troiano G, Perrone D, Dioguardi M, Buonavoglia A, Ardito F, Lo Muzio L. In vitro evaluation of the cytotoxic activity of three epoxy resin-based endodontic sealers. Dent Mater J 2018;37(3):374-8.
Cintra LTA, Benetti F, de Azevedo Queiroz IO, Ferreira LL, Massunari L, Bueno CRE y cols. Evaluation of the Cytotoxicity and Biocompatibility of New Resin Epoxy-based Endodontic Sealer Containing Calcium Hydroxide. J Endod 2017;43(12):2088-92.
Silva Almeida LH, Moraes RR, Morgental RD, Pappen FG. Are Premixed Calcium Silicate-based Endodontic Sealers Comparable to Conventional Materials? A Systematic Review of In Vitro Studies. J Endod 2017;43(4):527-35.
Camps J, Jeanneau C, El Ayachi I, Laurent P, About I. Bioactivity of a Calcium Silicate-based Endodontic Cement (BioRoot RCS): Interactions with Human Periodontal Ligament Cells In Vitro. J Endod 2015;41(9):1469-73.
Camps J, About I. Cytotoxicity testing of endodontic sealers: a new method. J Endod 2003;29(9):583-6.
Nussler A, Konig S, Ott M, Sokal E, Christ B, Thasler W y cols. Present status and perspectives of cell-based therapies for liver diseases. J Hepatol 2006;45(1):144- 59.
Rodrigues C, Costa-Rodrigues J, Capelas JA, Fernandes MH. Longterm dose- and time-dependent effects of endodontic sealers in human in vitro osteoclastogenesis. J Endod 2013;39(6):833-8.
Miletic I, Devcic N, Anic I, Borcic J, Karlovic Z, Osmak M. The Cytotoxicity of RoekoSeal and AH Plus Compared during Different Setting Periods. J Endod. 2005;31(4):307-9.
Taraslia V, Anastasiadou E, Lignou C, Keratiotis G, Agrafioti A, Kontakiotis EG. Assessment of cell viability in four novel endodontic sealers. Eur J Dent 2018;12(2):287-91.
Azar NG, Heidari M, Bahrami ZS, Shokri F. In vitro cytotoxicity of a new epoxy resin root canal sealer. J Endod 2000;26(8):462-5.
Huang FM, Tai KW, Chou MY, Chang YC. Cytotoxicity of resin-, zinc oxide– eugenol-, and calcium hydroxide-based root canal sealers on human periodontal ligament cells and permanent V79 cells. Int Endod J 2002;35:153.
Poggio C, Riva P, Chiesa M, Colombo M, Pietrocola G. Comparative cytotoxicity evaluation of eight root canal sealers. J Clin Exp Dent 2017;9(4):e574-e8.
Colombo M, Poggio C, Dagna A, Meravini MV, Riva P, Trovati F y cols. Biological and physico-chemical properties of new root canal sealers. J Clin Exp Dent 2018;10(2): e120-e6.
Bouillaguet S, Wataha JC, Tay FR, Brackett MG, Lockwood PE. Initial in vitro biological response to contemporary endodontic sealers. J Endod 2006;32(10):989-92.
Cotti E, Petreucic V, Re D, Simbula G. Cytotoxicity evaluation of a new resinbased hybrid root canal sealer: an in vitro study. J Endod 2014;40(1):124-8.
Vouzara T, Dimosiari G, Koulaouzidou EA, Economides N. Cytotoxicity of a New Calcium Silicate Endodontic Sealer. J Endod 2018;44(5):849-52.
Jung S, Sielker S, Hanisch MR, Libricht V, Schafer E, Dammaschke T. Cytotoxic effects of four different root canal sealers on human osteoblasts. PLoS One. 2018;13(3): e0194467.
Zhang W, Li Z, Peng B. Ex vivo cytotoxicity of a new calcium silicatebased canal filling material. Int Endod J 2010;43(9):769-74.
Van Landuyt KL, Geebelen B, Shehata M, Furche SL, Durner J y cols. No evidence for DNA double-strand breaks caused by endodontic sealers. J Endod 2012;38:636-641.
Shon WJ, Bae KS, Baek SH, Kum KY, Han AR, Lee WC. Effects of calcium phosphate endodontic sealers on the behavior of human periodontal ligament fibroblasts and MG63 osteoblast-like cells. J Biomed Mater Res B Appl Biomater 2012;100(8):2141-7.
Schutte RJ, Xie L, Klitzman B, Reichert WM. In vivo cytokine-associated responses to biomaterials. Biomaterials 2009;30(2):160-8.
Balto K, Sasaki H, Stashenko P. Interleukin-6 deficiency increases inflammatory bone destruction. Infect Immun 2001;69(2):744-50.
Jeanneau C, Giraud T, Laurent P, About I. BioRoot RCS Extracts Modulate the Early Mechanisms of Periodontal Inflammation and Regeneration. J Endod 2019;45(8):1016-1023.
Silva PT, Pappen FG, Souza EM, Dias JE, Bonetti Filho I, Carlos IZ y cols. Cytotoxicity Evaluation of Four Endodontic Sealers. Braz Dent J 2008;19(3):228-31.

Freire Mancebo, Yolanda
Profesora ayudante del Departamento de Odontología pre-clínica de la Universidad Europea.
Larrosa Pérez, Mar
MASMicrobiota Group. Profesora titular de Biotecnología Alimentaria de la Universidad Europea. Beca del programa Ramón y Cajal (2012_11910) del Ministerio de Economía y Competitividad, España.
Esteban Martínez, Isabel
MASMicrobiota Group. Facultad de Ciencias de la Salud de la Universidad Europea.
Palma White, Beatriz
Máster de Endodoncia Avanzada de la Universidad Europea.
Cisneros Cabello, Rafael
Catedrático del Departamento de Odontología Clínica y director del Máster de Endodoncia Avanzada de la Universidad Europea.